Coronaires
Publié le 30 nov 2015Lecture 8 min
Test de provocation au Méthergin® négatif… so what ?
M.-A. ARNOULD, Cardiologie interventionnelle, Clinique Saint-Gatien, Tours
Nous rapportons le cas d’une patiente de 53 ans, hospitalisée pour bilan de douleurs thoraciques. Son seul antécédent notable est une angioplastie de l’IVA proximale en 2002. Tous ses facteurs de risque sont contrôlés, avec un cholestérol LDL à 0,9 g/l sous 40 mg d’atorvastatine, en plus de 75 mg de Kardegic® et 5 mg de bisoprolol. Depuis 2002, Il n’y a eu aucun événement clinique jusqu’à ses dernières vacances estivales en 2015, au cours desquelles elle a présenté 3 épisodes angineux trinitro-sensibles, difficiles à caractériser à l’interrogatoire mais plutôt au repos, et avec au moins une syncope d’après son mari. Elle a alors été brièvement hospitalisée, avec une cinétique de la troponine US normale, et une échographie cardiaque d’effort maximal sans ischémie échographique ou clinique, mais avec apparition d’une tachycardie ventriculaire non soutenue (TVNS) à l’acmé de l’effort. Il n’y a pas eu de modification thérapeutique.
Elle nous est réadressée secondairement par son cardiologue en raison d’un nouvel épisode angineux de repos trinitro-sensible.
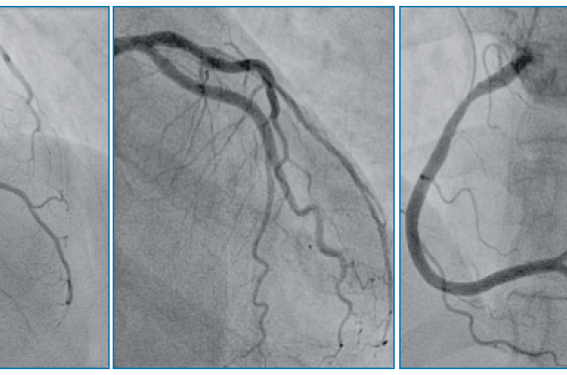
La coronarographie réalisée par voie radiale gauche (4F) confirme une bonne perméabilité du stent de l’IVA, avec une prolifération non significative, une CX indemne de lésion, et une lésion non significative de la CD I (figure 1). Nous avons alors réalisé dans la foulée un test de provocation au Méthergin® par voie veineuse (0,4 mg) qui s’est avéré négatif cliniquement, angiographiquement et électriquement (figure 2).
Figure 1. Réseau coronaire avant injection de Méthergin®.
Figure 2. Réseau coronaire 3 minutes après injection de 0,4 mg de Méthergin® IVD.
Dans l’attente de la réalisation d’une fibroscopie gastrique, nous avons poursuivi le même traitement, en contrôlant l’échographie cardiaque d’effort qui cette fois s’est avérée normale. Elle a de plus bénéficié de la pose d’un holter-ECG après sa coronarographie, pour s’assurer de l’absence d’explication rythmologique à sa syncope, d’autant plus qu’il avait été constaté une TVNS à l’échographie d’effort initiale. Le lendemain matin, la patiente a de nouveau présenté une douleur thoracique au repos, durant 1 à 2 minutes, trinitro-sensible, avec un ECG réalisé en postcritique normal. La fibroscopie gastrique a mis en évidence une gastrite banale, n’expliquant pas à elle seule les symptômes.
À la lecture du Holter-ECG, il a été constaté un sus-décalage transitoire du segment ST concomitant de la douleur survenue dans le service, avec bradycardie sinusale associée et ESV (figure 3).
Nous avons donc retenu le diagnostic d’angor de Prinzmetal.
Le traitement médical a été modifié avec introduction d’inhibiteurs calciques et de dérivés nitrés, et arrêt des bêtabloquants. La patiente a rejoint son domicile en l’absence de nouvel événement après 48 heures de surveillance en soins intensifs.
Figure 3. Holter ECG, avec sus-décalage du ST et ESV.
Discussion
Nous avons donc ici un cas typique d’angor de Prinzmetal tel qu’il a été décrit an 1959(1) (sus-décalage transitoire du segment ST associé à une douleur angineuse de repos, alors que l’effort est bien toléré). Bien que le spasme coronaire soit une entité bien décrite et connue, se pose ici le problème de son diagnostic, et notamment de la pertinence des tests de provocation. Même si la maladie coronaire athéromateuse est la cause la plus fréquente d’ischémie myocardique, le spasme coronaire en est une cause plus rare mais bien connue. La présentation clinique peut en être variée (angor de repos, SCA, mort subite, ou encore syncope). Nous ne discuterons pas ici de la prévalence, de la physiopathologie, ou encore des facteurs favorisants et du traitement du spasme. Ils sont en effet bien décrits, même si la compréhension de tous les mécanismes intervenants n’est pas toujours totale. Dépister et poser le diagnostic d’angor spastique est un véritable défi auquel nous sommes régulièrement confrontés dans notre pratique quotidienne.
Il est aisé de poser le diagnostic lorsqu’il est constaté sur un ECG, un holter-ECG ou un monitorage du ST, une élévation transitoire du segment ST associée à une douleur thoracique. Une épreuve d’effort(2), ou encore une manoeuvre d’hyperventilation(3). Toutefois, il a été montré que l’utilisation d’agents pharmacologiques rendait beaucoup plus sensible le dépistage du spasme(4). C’est pourquoi, la méthode de dépistage « invasive » du spasme coronaire est devenue la méthode la plus communément utilisée. Le recours au test de provocation est plus ou moins fréquent, selon les pays, les centres, et les praticiens, et sa pratique fait l’objet de recommandations (classe I en Asie où la prévalence du spasme est la plus élevée(5), grade IIA C en Europe(6)). Deux drogues permettent de provoquer un spasme coronaire, un dérivé de l’ergot de seigle, le Méthergin®, et l’acétylcholine (AC). Quelle que soit la drogue utilisée, son injection doit se faire au cours d’une coronarographie, pour éliminer, d’une part, une sténose coronaire significative (qui serait alors une contre-indication à l’injection d’une drogue vasospastique) et, d’autre part, pour pouvoir injecter en intracoronaire des dérivés nitrés en cas de spasme induit, qui serait réfractaire au dérivés nitrés sublinguaux. L’injection intraveineuse (IV) de Méthergin® à doses progressives au lit du patient comme elle a pu être pratiquée par le passé, — que le statut coronaire soit connu ou non —, doit donc être proscrite.
De nombreux protocoles ont été décrits pour ces deux molécules (tableau). Le test est considéré comme positif en cas de susdécalage du ST avec douleur thoracique et/ou de réduction significative de calibre d’au moins 75 % d’une ou plusieurs coronaires(7) (critère plus sévère en Asie avec au moins 90 % de réduction de calibre). Le Méthergin® peut être injecté par voie IVD ou intracoronaire (IC). Relativement simple à réaliser en IVD, il consiste à injecter 0,4 mg de Méthergin® (2 ampoules), puis de réaliser une angiographie coronaire 3 minutes après l’injection. Sa sensibilité et sa spécificité sont excellentes(8) et comparables à celles de l’injection IC(9) même si une étude à montrer une fréquence plus importante de tests positifs après injection IC(10).
ER : ergonovine maléate ; IV : intraveineuse ; IC : intracoronaire ; ACG : artère coronaire gauche ; ACD : artère coronaire droite ; SSN : solution saline normale ; NA : non applicable.
Le principal inconvénient de la voie IV est le risque d’un spasme diffus, pouvant toucher à la fois le réseau coronaire gauche et droit, pourvoyeur d’instabilité hémodynamique, accentuée par les dérivés nitrés IC nécessaires pour lever le spasme. Certaines équipes lui préfèrent donc la voie IC. L’injection se fait de façon sélective à doses progressives pour la coronaire gauche (jusqu’à 60 μg) et la coronaire droite (jusqu’à 60 μg). Un contrôle coronarographique de la coronaire étudiée est effectué avant de procéder à l’injection controlatérale de Méthergin®. Il convient de respecter un délai de quelques minutes entre chaque injection. L’injection IC sélective permet d’éviter un spasme diffus, mais nécessite plus de temps que la voie IV.
Le test de provocation à l’AC se fait de la même façon que l’injection IC de Méthergin®. Elle est contre-indiquée en cas d’insuffisance respiratoire. La dose cible est de 200 μg pour chaque coronaire.
Comme l’a confirmé en 2015 une étude rétrospective(11) (21 500 patients ayant bénéficié d’un test de provocation, le risque de survenue d’événements indésirables graves est extrêmement faible pour l’un ou l’autre des tests (1 seul décès, 4 poses de ballon de contrepulsion, 126 troubles du rythme nécessitant un choc électrique externe). Les troubles du rythme ont été significativement plus fréquents avec l’AC. Les bradycardies sévères ou troubles de la conduction après AC sont habituellement bénins(12). Cette étude confirme les données d’autres études prospectives préalables(13). À condition d’avoir un accès intracoronaire pour injection de nitrés si besoin — les décès induits par spasme réfractaire après injection IV de Méthergin® ayant été rapportés après injection au lit du patient — l’injection IV de Méthergin® ne présente pas plus de risque d’événements indésirables sévères(14).
Bien qu’une étude ait montré une différence significative en faveur de l’AC en termes de sensibilité et de spécificité(15), les résultats de la plupart des études s’accordent sur le fait que les deux tests (AC et Méthergin®) sont globalement comparables(16). Il en est de même pour la voie d’abord choisie pour l’injection de Méthergin® (IV ou IC), à quelques exceptions près déjà citées. Toutefois, malgré leur excellente sensibilité et spécificité, il a été décrit des cas d’angor spastique alors même que les tests de provocation étaient négatifs(17), ce qui est le cas de dossier clinique.
Plusieurs pistes de réflexion peuvent alors être avancées. La première est directement liée à une évolution majeure de la cardiologie interventionnelle depuis les années 2000. En effet, la voie radiale est désormais la voie d’abord de première intention en France pour réaliser une coronarographie. Celle-ci implique l’injection dans l’artère radiale de dérivés nitrés et/ou d’inhibiteurs calciques en début de procédure pour se prémunir du spasme de celle-ci. Nous injectons dans notre centre 1 mg de Risordan® en intraartériel en plus d’une petite dose d’héparine après la pose du désilet, or, ce sont les antidotes du Méthergin® ou de l’AC. Il n’existe bien sûr pas d’étude ayant comparé les résultats d’un test de provocation par voie radiale et par voie fémorale (donc sans injection de vasodilatateurs préalables) sur un même patient. Mais, en plus de l’effet local sur l’artère radiale, il existe nécessairement une action vasodilatatrice systémique — et donc coronaire —, en témoignent les hypotensions parfois constatées en début de coronarographie. De plus, la durée de réalisation d’une coronarographie étant actuellement de quelques minutes, il est légitime de se poser la question du caractère « démaquillé » ou non du test de provocation lorsqu’il est débuté.
Nous n’avons pas repris la patiente pour un test de provocation par voie fémorale, puisque le diagnostic est certain chez elle. Cependant, de rares indications comme la persistance de symptômes chez un patient spastique connu sous traitement, ou bien avant arrêt du traitement antispastique, peuvent justifier d’un abord fémoral. Concernant notre patiente, nous réaliserons un test de provocation sous traitement par voie fémorale en cas de récidive angineuse. L’idée d’un abord radial sans injection préalable de vasodilatateurs pour la réalisation d’un test de provocation est utopique, le spasme radial étant un obstacle à la réalisation du cathétérisme.
Bien que les différents tests de provocation soient comparables, en attestent les recommandations qui laissent libre choix de l’un ou l’autre, nous avons rappelé qu’une étude a démontré la supériorité de l’injection IC de Méthergin® comparativement à l’injection IV, tout comme l’AC comparativement au Méthergin® IC. Compte tenu des incertitudes liées à l’effet masquant potentiel des vasodilatateurs injectés par voie radiale dont nous avons discuté, le choix de l’AC en première intention peut se discuter, sauf contre-indication, mais au prix d’un risque de troubles du rythme plus élevé, et d’une procédure beaucoup plus longue que l’injection IV de Méthergin®. Il serait nécessaire d’avoir plus de données statistiques pour l’affirmer. La réalisation d’un test de provocation par voie fémorale lors d’une procédure ultérieure reste une solution envisageable si le diagnostic formel d’angor spastique s’impose et en cas de forte présomption clinique.
En pratique
Ce cas clinique rappelle que le spasme coronaire existe, qu’il faut savoir l’évoquer et le dépister.
Si un test de provocation anormal permet de poser le diagnostic, un test de provocation normal n’élimine pas formellement un angor de Prinzmetal.
Il faut savoir le traiter si la présomption clinique est forte, d’autant que les inhibiteurs calciques non bradycardisants sont en général peu pourvoyeurs d’effets secondaires, en insistant tout particulièrement sur l’arrêt impératif du tabagisme.
Attention, pour des raisons réglementaires ce site est réservé aux professionnels de santé.
pour voir la suite, inscrivez-vous gratuitement.
Si vous êtes déjà inscrit,
connectez vous :
Si vous n'êtes pas encore inscrit au site,
inscrivez-vous gratuitement :