Publié le 01 jan 2018Lecture 4 min
Durabilité des bioprothèses aortiques percutanées
Julien DREYFUS, Centre Cardiologique du Nord, Saint-Denis
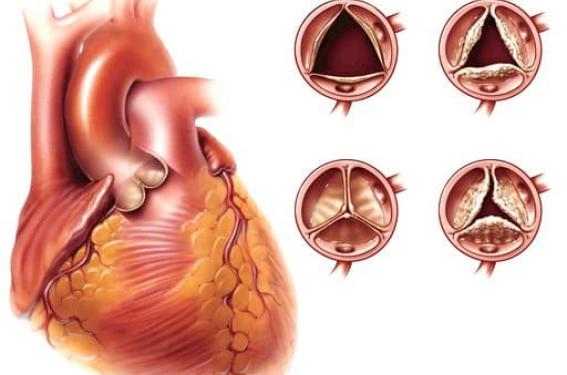
Le nombre de bioprothèses aortiques implantées par voie percutanée (TAVI) augmente de façon significative chaque année (déjà plus de 300 000 procédures réalisées dans le monde) et devrait s’accroître à l’avenir avec l’élargissement de ses indications. Un des éléments essentiels à déterminer pour la poursuite du développement de cette procédure est la durabilité des bioprothèses ainsi mises en place.
Une technique récente
Il s’agit en effet d’une technique récente avec une première procédure en 2002, un marquage européen en 2007 et américain en 2011, pour laquelle nous disposons de peu de recul. De plus, son évaluation actuelle est biaisée car les études offrant un recul > 5 ans portent sur les prothèses de première génération implantées par des opérateurs inexpérimentés avec donc plus de prothèses mal positionnées, de mauvais choix de taille de prothèse et de fuites périprothétiques post-procédurales.
Enfin, ces prothèses ont initialement été implantées chez des patients très âgés avec de multiples comorbidités et une espérance de vie limitée qui ne permet pas d’étude sur du long terme.
Malgré toutes ces limites, les performances de ces bioprothèses à 5 ans, en termes d’hémodynamique et de surface, semblent au moins équivalentes à celles implantées par voie chirurgicale.
La durabilité des bioprothèses est surtout liée à la dégénérescence structurelle de la valve (DSV), qui est inéluctable, aboutissant à une dysfonction progressive de la bioprothèse sur un mode sténosant, fuyant ou les deux.
La dégénérescence de la prothèse
Il est important de souligner qu’il est fondamental d’avoir une définition consensuelle et universelle de cette DSV, ce qui a été récemment proposé par les sociétés savantes européennes(1). Des critères échocardiographiques ont été retenus, hémodynamiques (un gradient moyen transprothétique > 20 mmHg et/ou ou une augmentation de plus de 10 mmHg comparativement à l’échocardiogramme réalisé dans les 30 jours suivant l’intervention, l’apparition ou la majoration d’une fuite intraprothétique) et morphologiques (anomalies de l’intégrité et/ou de la mobilité des feuillets, anomalies de l’armature/stent).
Les mécanismes des DSV connus pour les bioprothèses sont multiples, le principal étant l’apparition de calcifications valvulaires qui vont dégrader les feuillets.
Ces calcifications sont favorisées par le traitement au glutaraldéhyde des prothèses (qui a pour but de diminuer les rejets en rendant les prothèses « immunologiquement inertes »), les anomalies du métabolisme phospho-calcique (insuffisance rénale, hyperparathyroïdie), le stress hémodynamique/ mécanique sur les feuillets (HTA, mismatch) et possiblement les thromboses de prothèses (même infracliniques).
Les facteurs favorisant la DSV sont le jeune âge, les facteurs de risque cardiovasculaire, l’insuffisance rénale chronique, la persistance d’une hypertrophie ventriculaire gauche, une petite taille de prothèse et un mismatch. Nous ne disposons à ce jour d’aucun traitement pour prévenir ces DSV.
Il existe des facteurs favorisant les DSV spécifiques aux bioprothèses aortiques percutanées, qui sont principalement liés à la procédure. Ainsi, la compression de la prothèse, d’autant plus importante avec le temps que la tendance est à la miniaturisation des gaines pour les abords vasculaires, est responsable de lésions tant au niveau des feuillets que du stent (figure 1).
Figure 1. Lésions induites par la compression per-procédurale de la prothèse. La prothèse (3 feuillets dans un stent) est comprimée avant d’être introduite dans le patient, le plus souvent par voie endovasculaire artérielle fémorale (A). Lésions des feuillets de la prothèse (B, flèche blanche) favorisant des phénomènes prothrombotiques caractérisés ici par des amas de cellules sanguines (C).
D’après Khoffi F et al. J Biomed Mater Res 2014 ; Bourget JM et al. Morphologie 2017.
De même, l’expansion imparfaite de la prothèse (déploiement sous-optimal, anomalies d’angle ou de hauteur), liée au fait que les calcifications sont asymétriques, limite l’obtention d’une prothèse bien circulaire (figure 2) (à la différence des bioprothèses implantées chirurgicalement après exérèse de la valve pathologique et des calcifications), ce qui majore le stress hémodynamique (en plus d’éventuelles fuites périprothétiques).
Enfin, il a été rapporté une prévalence non négligeable de thromboses intracliniques de prothèses qui pourraient favoriser les DSV.
Figure 2. Expansion imparfaite de la prothèse. Calcifications asymétriques de la valve aortique native (A). Prothèse de TAVI circulaire (B). Déploiement de la bioprothèse dans la valve aortique calcifiée (C). Après déploiement, la prothèse n’est pas complètement circulaire (D).
D’après Morganti S et al. Journal of Biomechanics 2014.
Une thérapeutique en expansion
Le TAVI est donc une thérapeutique de plus en plus séduisante, mais la poursuite du développement de cette technique et de l’élargissement de ses indications, surtout pour des sujets plus jeunes, dépendra beaucoup de sa durabilité, principalement liée à la DSV.
Il faudra ainsi du temps pour pouvoir répondre à cette interrogation, mais les résultats sont pour le moment encourageants.
Attention, pour des raisons réglementaires ce site est réservé aux professionnels de santé.
pour voir la suite, inscrivez-vous gratuitement.
Si vous êtes déjà inscrit,
connectez vous :
Si vous n'êtes pas encore inscrit au site,
inscrivez-vous gratuitement :






