Publié le 08 avr 2008Lecture 7 min
Endocardites aiguës : ce que le clinicien doit savoir
J.-Ch. EICHER, Centre de Cardiologie Clinique et Interventionnelle, CHU Dijon
L’endocardite aiguë, par opposition à l’endocardite subaiguë ou maladie d’Osler, se caractérise par un terrain souvent débilité, l’absence de valvulopathie préexistante connue, des germes très agressifs, un tableau clinique bruyant, et une morbi-mortalité élevée. L’échocardiogramme possède un rôle crucial pour le diagnostic lésionnel, la stratification du risque, et la stratégie thérapeutique. La chirurgie précoce est aujourd’hui recommandée dans certaines situations, et améliore le pronostic de cette pathologie redoutable.
Deux formes cliniques
Il est classique de distinguer l’endocardite subaiguë ou lente, ou maladie d’Osler, se développant à bas bruit sur une cardiopathie préexistante, où les agents infectieux responsables relativement peu virulents sont dominés par les streptocoques non groupables (Str. viridans), de l’endocardite aiguë. Même si cette dichotomie paraît aujourd’hui un peu artificielle, elle a le mérite didactique de séparer deux formes cliniques d’endocardite infectieuse au profil évolutif et au pronostic radicalement différents (tableau 1).
Par opposition à l’endocardite subaiguë, la forme aiguë survient en principe en l’absence de valvulopathie préexistante, le germe responsable est hautement virulent (staphylocoque le plus souvent), son tableau clinique est bruyant (syndrome infectieux sévère) et rapidement évolutif vers des complications graves (destructions valvulaires, insuffisance cardiaque, abcès de l’anneau, embolies et foyers infectieux métastatiques), son pronostic est sévère.
Ainsi, pour décrire l’endocardite aiguë, on peut retenir trois rubriques caractéristiques fondamentales et les détailler successivement :
- il s’agit généralement d’une endocardite à staphylocoque ;
- les valves sont considérées comme initialement saines ;
- le caractère aigu est synonyme de sévérité.
Spécificité des endocardites à staphylocoque
Les staphylocoques sont impliqués dans une proportion croissante d’endocardites infectieuses (EI) : 29 % en France selon l’Association pour l’étude et la prévention de l’endocardite infectieuse en 2002 (AEPEI)(1). St. aureus est considéré comme extrêmement virulent, mais certains staphylocoques coagulase négative comme St. lugdunensis ont récemment été identifiés comme responsables d’EI agressives(2).
L’étude de l’équipe d’Amiens(3) a montré que les endocardites à St. aureus sont caractérisées par un terrain particulier (comorbidités sévères, insuffisants rénaux et hémodialysés), une évolutivité plus rapide (durée des symptômes plus courte avant diagnostic), une prévalence plus élevée d’atteintes du cœur droit, un taux plus élevé de complications graves (accidents neurologiques majeurs, défaillance multi-viscérale), et une mortalité plus élevée (34 vs 10 %) que lorsqu’un autre germe est impliqué.
D’une façon générale, la plupart des études sont concordantes sur le fait que l’infection à staphylocoque représente un facteur indépendant de gravité, systématiquement associé à un risque accru d’accidents emboliques(4), d’abcès annulaires, et de mortalité hospitalière(4,5).
Absence de cardiopathie préexistante
Il s’agit d’une situation plus fréquente qu’on ne le croit habituellement. L’AEPEI a évalué à 47 % la proportion de patients qui n’étaient pas porteurs d’une cardiopathie connue au moment du diagnostic d’EI.
L’absence de valvulopathie préexistante est une notion qu’il convient de nuancer : il serait plus correct de parler d’absence de régurgitation préexistante. Dans ce cadre, l’endocardite du cœur droit du toxicomane représente un modèle quasi « expérimental » : en l’absence de lésions structurelles préexistantes, l’endocarde de la tricuspide est colonisé en raison d’un inoculum massif et répété de germes hautement virulents. Il peut néanmoins exister de façon méconnue des lésions mineures telles qu’une bicuspidie aortique. Il faut y associer les endocardites survenant sur lésions dégénératives relativement silencieuses, telles que les calcifications de l’anneau mitral (CAM) : ce type d’atteinte est peu reconnu car difficile à distinguer des endocardites valvulaires mitrales classiques (figure 1) ; sa prévalence est pourtant en augmentation, survenant préférentiellement chez les hémodialysés et les sujets âgés(6).
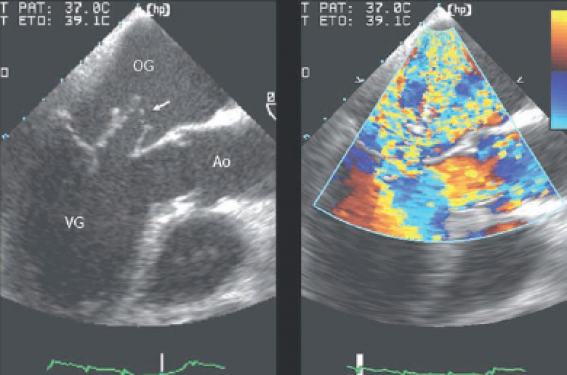
Figure 1. ETO, incidence 110°. À gauche, volumineuse végétation sur anneau mitral calcifié. Au centre et à droite, contrôle à 3 semaines : disparition de la végétation, cavité annulaire abcédée, fistulisée dans l’oreillette gauche (A : abcès ; Ao : aorte ; CAM : calcification de l’anneau mitral ; OG : oreillette gauche ; V : végétation ; VG : ventricule gauche ; VMA : valve mitrale antérieure ; VMP : valve mitrale postérieure).
Les endocardites survenant sur prothèse valvulaire peuvent artificiellement être qualifiées d’aiguës, dans la mesure où le profil évolutif est tout à fait comparable. Enfin, les aortites infectieuses, même si elles sont rares, peuvent entrer dans ce cadre : anévrismes mycotiques sur plaques athéromateuses(7), ou sur coarctation.
Gravité des endocardites aiguës
Le terme « aigu » possède implicitement une connotation péjorative car l’évolution rapide expose à des complications : destruction valvulaire, désinsertion prothétique, abcès annulaires ou myocardiques, fistules, péricardite purulente ou infections métastatiques.
Parmi les complications de l’EI, l’insuffisance cardiaque est celle qui présente l’impact le plus lourd sur le pronostic(8). Elle est plus fréquente et moins bien tolérée en cas d’endocardite intéressant l’orifice aortique. L’échocardiogramme permet d’évaluer le retentissement hémodynamique (taille des cavités, fonction ventriculaire gauche, pressions pulmonaires et de remplissage), de préciser le mécanisme de la défaillance cardiaque (régurgitation sévère, végétations obstructives, ischémie par embolie coronaire ou compression par un abcès annulaire, fistule intracardiaque), et de réaliser une analyse descriptive précise (perforations, déchirures, rupture de cordage, désinsertion prothétique, extension péri-annulaire) qui va aider à établir une stratégie chirurgicale (figure 2).
Figure 2. ETO, incidence 120°. Anévrysme mycotique du feuillet mitral antérieur multiperforé (Ao : aorte ; OG : oreillette gauche ; VG : ventricule gauche).
Les complications emboliques comportent également une redoutable importance pronostique. Elles surviennent dans 22 à 50 % des cas, impliquent le système nerveux central 2 fois sur 3(8), et sont plus fréquentes avec certains germes, notamment le staphylocoque doré et les Candida. La majorité des événements emboliques surviennent au cours des 2 premières semaines de traitement antibiotique. Le risque embolique peut être prédit par l’échocardiographie.
Si certaines publications ont évoqué un nombre plus élevé d’événements en cas d’atteinte mitrale, d’autres comme celle de l’équipe de Marseille ont démontré qu’en analyse multivariée seules la taille et la mobilité des végétations étaient prédictives(9). Ces résultats ont été confirmés par une étude multicentrique française : Staphylococcus aureus et Streptococcus bovis sont significativement associés au nombre total d’événements emboliques, alors que les nouveaux événements sont prédits par une végétation de taille > 10 mm et de mobilité sévère ; la taille de la végétation > 15 mm représente en analyse multivariée un facteur de mortalité indépendant des autres avec un risque relatif de 1,8(4).
L’extension périannulaire est un facteur prédictif de mortalité (41 %), d’insuffisance cardiaque (62 %) et de chirurgie précoce. L’échocardiographie transœsophagienne (ETO) représente la modalité de choix pour le diagnostic de cette complication (recommandation de classe IA pour l’AHA)(8). Elle survient dans 10 à 40 % des endocardites sur valve native (presque toujours sur l’orifice aortique), et dans 56 à 100 % des endocardites prothétiques. La plupart des infections annulaires impliquant l’orifice mitral sont l’apanage des prothèses(8) ; dans la rare éventualité d’un abcès de l’anneau mitral sur valve native, il convient d’évoquer une contamination directe de l’anneau par l’intermédiaire d’une CAM(6).
Lorsque l’abcès annulaire, initialement cavité purulente circonscrite, entre en communication avec la lumière orificielle, il devient par définition un anévrisme mycotique.
Dès lors, cette cavité se retrouve soumise aux pressions systémiques et va s’expandre (aboutissant parfois à une véritable discontinuité ventriculo-aortique), voire progresser par des trajets fistuleux jusqu’aux autres cavités cardiaques (figure 3). Cette complication est encore une fois l’apanage quasi exclusif des endocardites aortiques ; les fistules aorto-cavitaires surviennent dans 1,8 % des endocardites sur valve native et 3,5 % des endocardites prothétiques. La sensibilité diagnostique de l’ETO est, là encore, supérieure à celle de l’examen transthoracique (97 vs 53 %). Le point de départ concerne les 3 sinus de Valsalva à fréquence équivalente, aboutissant à l’une des 4 cavités cardiaques sans distinction. Ces données sont solidement étayées par l’étude multicentrique française sur les abcès périvalvulaires(10) et les travaux du groupe de travail hispano-américain sur les fistules aorto-cavitaires(11).
Figure 3. ETO, incidence 120°. Abcès du trigone aorto-mitral (astérisque) fistulisé dans l’oreillette gauche (flèche) (Ao : aorte ; CCVG : chambre de chasse du ventricule gauche ; OG : oreillette gauche).
Indications pour une chirurgie précoce
Classiquement, une intervention chirurgicale précoce en phase septique est considérée comme à plus haut risque en raison des difficultés techniques et de la crainte d’une reprise du processus infectieux sur la prothèse. En réalité, la durée du traitement antibiotique avant la chirurgie ne semble pas influer sur la mortalité périopératoire(12). Au contraire, il existe de nombreux arguments dans la littérature pour dire que la chirurgie précoce dans des sous-groupes de patients sélectionnés améliore significativement le pronostic de cette pathologie redoutable(12,13).
Les recommandations européennes(15), comme les américaines plus récentes(16), sont en faveur d’une chirurgie rapide en cas d’insuffisance cardiaque, de résistance au traitement antibiotique, ou d’extension périannulaire (tableaux 2 et 3). Les endocardites fongiques et à staphylocoque doré, ainsi que les EI précoces (< 12 mois) sur prothèse, sont presque toujours chirurgicales. La décision sur la base de l’aspect et de la taille des végétations est plus controversée, en sachant que le risque de récidive après un premier événement est élevé, et qu’une chirurgie préventive n’est pas contre-indiquée si elle est pratiquée rapidement (< 72 heures) et que le scanner ne montre pas de signes hémorragiques(12,15).
En pratique
L’endocardite aiguë est une pathologie redoutable grevée d’une morbi-mortalité élevée. L’échocardiogramme transthoracique et transœsophagien est l’examen clé possédant une importance indiscutable dans le diagnostic, la surveillance, l’évaluation pronostique et la prise de décision.
Attention, pour des raisons réglementaires ce site est réservé aux professionnels de santé.
pour voir la suite, inscrivez-vous gratuitement.
Si vous êtes déjà inscrit,
connectez vous :
Si vous n'êtes pas encore inscrit au site,
inscrivez-vous gratuitement :






