Échocardiographie
Publié le 01 fév 2005Lecture 9 min
Évaluation non invasive de la reperfusion par échographie de contraste
E. BROCHET, hôpital Bichat, Paris
Les traitements de reperfusion, qu’il s’agisse de thrombolyse ou d’angioplastie primaire, ont permis d’améliorer considérablement le pronostic des patients présentant un infarctus du myocarde (IDM). Des limites persistent cependant à la fois dans l’efficacité de ces traitements et dans les moyens d’identifier avec précision le succès de la reperfusion. L’importance pronostique d’une reperfusion myocardique complète est un fait bien établi. Celle-ci n’est appréciée que très imparfaitement par les techniques angiographiques. Des méthodes plus sensibles sont nécessaires pour évaluer la reperfusion à l’échelon microvasculaire myocardique. L’échographie de contraste myocardique (ECM) est une technique séduisante dans ce contexte, permettant l’exploration de la microcirculation myocardique après injection de microbulles.
Si l’échographie de contraste par voie intracoronaire a été la plus étudiée en phase aiguë d’IDM, lors des angioplasties primaires, le développement plus récent des techniques d’échographie de contraste par voie veineuse offre la possibilité d’une exploration non invasive de la reperfusion.
Il faut souligner d’emblée que cette technique n’est pas encore utilisée en routine, les agents de contraste n’ayant pas encore d’AMM pour l’étude de la perfusion myocardique. Cette approche a néanmoins été validée dans plusieurs travaux de recherche récents et semble prometteuse.
Agents de contraste
Les agents de contraste ultrasonores sont constitués de solutions de microbulles de gaz de petite taille, proche de celle des éléments figurés du sang, circulant librement dans la circulation sanguine et franchissant la barrière capillaire pulmonaire. Ces agents se différencient par le type de gaz contenu dans les microbulles et leur mode de stabilisation. Le gaz utilisé peut être de l’air, (Levovist®) ou un gaz lourd de type fluorocarbone pour les agents plus récents (Optison®, Sonovue®). L’intérêt des gaz fluorocarbonés est leur caractère peu diffusible, permettant d’obtenir des microbulles beaucoup plus stables et une opacification plus prolongée.
En France, on ne dispose encore que du Levovist® et du Sonovue® (ce dernier n’ayant pas d’AMM pour la phase aiguë de l’infarctus). D’autres agents de contraste sont actuellement en cours de développement ou de commercialisation.
Techniques de détection
Leur principe général consiste à rehausser le signal ultrasonore en provenance des microbulles, tout en essayant de réduire l’intensité du signal en provenance du myocarde. Différentes modalités sont actuellement disponibles, leurs performances dépendant pour une grande part des propriétés des agents de contraste utilisés.
Les méthodes d’imagerie dites destructives, utilisant des énergies acoustiques élevées, comme l’imagerie harmonique ou harmonic power doppler, nécessitent une acquisition intermittente des images, synchronisée à l’ECG (imagerie intermittente). Cette dernière technique est la plus adaptée aux agents de contraste fragiles comme Levovist®. L’intervalle de couplage entre les images peut être réglé de façon variable, permettant de quantifier le niveau de perfusion.
Les méthodes d’imagerie non destructives, ou imagerie de contraste en temps réel, utilisent de très faibles énergies acoustiques. Elles permettent une analyse simultanée de la cinétique et de l’opacification myocardique.
Renseignements apportés par l’échographie de contraste
L’opacification microvasculaire myocardique renseigne sur l’intégrité de la microcirculation et le volume sanguin myocardique, essentiellement composé de capillaires. Un des points forts de l’échographie de contraste est sa résolution spatiale, capable d’analyser la répartition transmurale du volume sanguin myocardique. L’opacification simple n’apporte, en revanche, aucune information sur le débit sanguin régional.
Des techniques de quantification ont été développées pour étudier le débit myocardique au sein des capillaires en échographie de contraste par voie veineuse. Celles-ci s’appuient sur l’utilisation du principe de destruction transitoire des microbulles, avec étude de leur réapparition au cours d’une perfusion continue à débit constant.
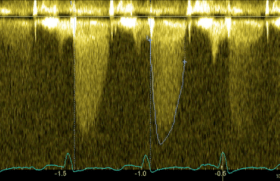
Elles peuvent être utilisées avec les techniques d’imagerie intermittente (figure 1), en faisant varier l’intervalle de trigger, ou plus facilement lors de l’imagerie temps réel, après un flash de destruction à forte énergie suivi d’une étude de la réapparition des microbulles en imagerie à basse énergie (séquence flash-reperfusion) Ces nouvelles techniques offrent la possibilité d’étudier plus finement les modifications microvasculaires induites par l’ischémie et la reperfusion.
Figure 1. Évaluation de la reperfusion en échographie de contraste après infarctus antérieur (technique d’imagerie intermittente harmonic power doppler avec Levovist®) (hôpital Bichat). À gauche, reperfusion complète 60 minutes après thrombolyse avec opacification homogène des différentes parois. À droite, échec de reperfusion myocardique avec présence d’un large défaut de perfusion apical (flèche).
Modifications microcirculatoires après reperfusion
Au cours de la reperfusion, la perfusion microvasculaire est très hétérogène, associant des zones de destruction microvasculaire, des zones de ralentissement circulatoire (low flow), des zones de flux normal et des zones d’hyperhémie. À cette hétérogénéité spatiale s’ajoute une hétérogénéité temporelle, avec des phénomènes dynamiques importants, surtout marqués dans les premières heures suivant la reperfusion. Les études expérimentales ont montré que ces phénomènes se stabilisaient environ 3 heures après la reperfusion et que l’évaluation des lésions microvasculaires était, à ce moment, bien corrélée à la taille de l’infarctus.
Dans les jours suivant la reperfusion, des modifications dynamiques peuvent encore s’observer, avec soit une aggravation des lésions microvasculaires, soit plus souvent une amélioration de celles-ci, suggérant une réversibilité partielle de la dysfonction microvasculaire.
Applications de l’ECM pour l’étude de la reperfusion
ECM en postthrombolyse
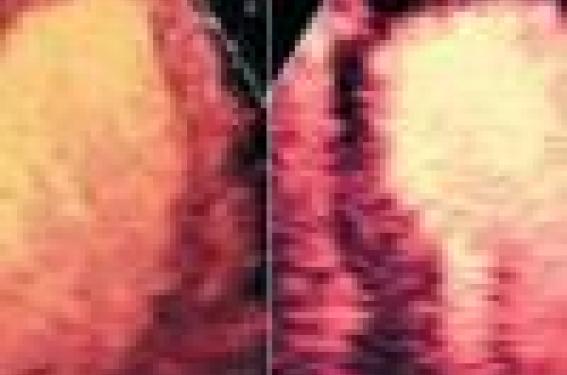
L’évaluation clinique et électrocardiographique du succès de la thrombolyse reste imparfaite. L’échographie de contraste par voie veineuse, réalisée dans les 30 à 60 minutes après thrombolyse, pourrait permettre d’en apprécier l’efficacité (figure 2).
Figure 2. Échocardiographie de contraste temps réel, utilisant un très faible index mécanique après injection intraveineuse de Sonovue® (Altana Pharma). Présence d’un défaut de perfusion apical dans les suites d’un infarctus antérieur (Power modulation Philips Ultrasons (gauche) et CPS Acuson Siemens (droite).
Cette approche n’a pour l’instant fait l’objet que de travaux assez préliminaires. Elle nécessite idéalement la réalisation d’une première échographie de contraste à l’admission, puis un second examen, réalisé immédiatement après le traitement de façon à comparer les images et apprécier la réduction de taille du défaut de perfusion.
Une opacification myocardique homogène témoignerait de la reperfusion complète au niveau myocardique. À l’opposé, la persistance d’un défaut de perfusion témoigne d’une absence de reperfusion.
Deux limites de cette approche doivent être connues :
• le risque de surestimer le degré de reperfusion myocardique en raison des phénomènes d’hyperhémie présents immédiatement après la reperfusion ;
• l’absence de corrélation étroite entre perméabilité coronaire et perfusion myocardique. Avant désobstruction coronaire, la perfusion peut être normale s’il existe une bonne collatéralité. Après reperfusion, la persistance d’un défaut de perfusion peut signifier soit un échec de désobstruction coronaire, soit un phénomène de no-reflow microvasculaire malgré une recanalisation coronaire complète.
Quoi qu’il en soit, l’intérêt de cette évaluation précoce par échographie de contraste serait de permettre une stratification précoce entre pa-tients à bas risque, présentant une opacification myocardique homogène et patients non reperfusés à haut risque de complications, présentant une absence de modification ou une faible réduction du défaut de perfusion. Cette stratification permettrait d’orienter les patients avec échec de reperfusion vers un traitement complémentaire, comme une angioplastie de sauvetage.
ECM après angioplastie primaire
L’intérêt de l’échographie de contraste est ici l’identification du phénomène de no-reflow. Celui-ci est défini par une absence de perfusion à l’échelon microvasculaire myocardique malgré une perméabilité coronaire angiographique. Les études réalisées en échographie de contraste intracoronaire ont mis en évidence la grande fréquence de ce phénomène, observé chez 30 à 40 % des patients traités avec succès par angioplastie primaire pour infarctus antérieur (flux TIMI 3). Sa fréquence atteint 90 à 100 % lorsque le flux coronaire angiographique est altéré (TIMI 2).
Son identification est également possible en échographie de contraste par voie veineuse, comme l’ont montré plusieurs études récentes. Le phénomène de no-reflow est défini par la présence après reperfusion d’un défaut d’opacification de plus de 25 % (50 % dans certaines études) de la zone à risque (zone akinétique ou zone non perfusée avant recanalisation coronaire si l’on dispose d’une échographie de contraste à l’admission). Selon la définition employée et le type de patients étudiés (patients complètement recanalisés [TIMI 3] ou non), la fréquence du phénomène de no-reflow est de l’ordre de 50 à 70 % par cette technique après infarctus du myocarde de topographie antérieure.
Ici encore, l’importance des phénomènes dynamiques doit être soulignée. Il est recommandé d’effectuer l’évaluation au moins 3 heures après la recanalisation coronaire pour limiter l’influence des phénomènes d’hyperhémie. En fait, le délai optimal exact d’évaluation n’est pas connu, certains proposant une évaluation plus tardive après 48 heures, paraissant plus prédictive de la récupération fonctionnelle. L’avantage particulier de la technique intraveineuse par rapport à la voie intracoronaire est la possibilité d’effectuer des examens de façon répétée, permettant d’apprécier les modifications temporelles de la reperfusion.
Signification des anomalies microcirculatoires observées
L’importance pronostique de la reperfusion myocardique complète, telle qu’elle peut être visualisée en ECM intracoronaire ou intraveineuse, a été démontrée dans de nombreuses études. L’intégrité de la microcirculation est une condition nécessaire à une récupération fonctionnelle ultérieure.
L’ECM apporte donc des informations très précoces sur l’existence d’une viabilité myocardique au sein de segments akinétiques.
Plusieurs points sont à souligner :
• l’absence d’opacification myocardique (no-reflow) est constamment associée à une évolution clinique péjorative, au remodelage ventriculaire gauche à distance, et est très prédictive d’une absence de viabilité ;
• si une opacification homogène traduit l’intégrité de la microcirculation, elle n’est pas toujours associée à une récupération fonctionnelle complète. Le degré de récupération dépend de l’extension transmurale de la nécrose, comme le suggère la bonne relation entre les données de l’ECM et la présence d’une réserve contractile sous dobutamine à distance. Même en l’absence de récupération fonctionnelle, une préservation partielle de l’intégrité microcirculatoire, notamment épicardique, peut être bénéfique pour limiter les phénomènes de remodelage à distance de l’infarctus ;
• les techniques de quantification de la perfusion, en ECM, récemment développées, semblent prometteuses pour mieux prédire la récupération fonctionnelle. Celles-ci permettent d’identifier des zones de flux myocardique présent mais très diminué, correspondant soit à une collatéralité soit à une zone de flux très lent, qui semblent les plus prédictives de récupération ;
• l’intérêt des examens répétés dans le postinfarctus a été souligné dans plusieurs travaux. Une amélioration de la perfusion en ECM au cours du suivi n’est pas exceptionnelle et est associée à une meilleure récupération fonctionnelle et à une évolution moins fréquente vers le remodelage.
Limites actuelles
Indépendamment des problèmes liés à la disponibilité des agents de contraste, la technique d’ECM connaît encore des limitations.
- La technique nécessite un apprentissage spécifique à la fois pour sa réalisation et son interprétation. La présence d’artefacts, fréquents dans les régions latérale et inférieure, doit être connue. Les meilleurs résultats sont obtenus pour le territoire antéroseptal.
- Les modalités d’injection du contraste, soit en bolus, soit en perfusion continue, font encore l’objet de débats.
- Enfin, la faisabilité de son utilisation en routine en phase aiguë d’infarctus et sa reproductibilité sont encore imparfaitement connues. L’échographie de contraste temps réel et l’avènement de nouveaux agents de contraste devrait améliorer cette faisabilité dans l’avenir, avec une utilisation sans doute plus facile des techniques de quantification.
En conclusion
L’échographie de contraste myocardique représente un outil très séduisant pour l’évaluation non invasive de la reperfusion.
Ses avantages principaux sont sa disponibilité au lit du malade en urgence, sa capacité à étudier à la fois la cinétique et la perfusion, et de répéter les examens au cours du suivi.
Cette technique pourrait permettre une stratification pronostique précoce, pouvant aider à sélectionner les patients qui nécessitent des traitements complémentaires et à évaluer le résultat de ces traitements à l’échelon microvasculaire.
Enfin, elle pourrait jouer un rôle important dans l’évaluation précoce de la viabilité.
Attention, pour des raisons réglementaires ce site est réservé aux professionnels de santé.
pour voir la suite, inscrivez-vous gratuitement.
Si vous êtes déjà inscrit,
connectez vous :
Si vous n'êtes pas encore inscrit au site,
inscrivez-vous gratuitement :