Cardiopathies congénitales
Publié le 26 avr 2009Lecture 16 min
Surveillance et traitement des grands enfants et des adultes opérés de tétralogie de Fallot
L. COHEN, T. HAZELZET, J. ZOGHBI et Y. LECOMPTE, Unité de Cardiologie Congénitale, Institut Hospitalier Jacques Cartier, Massy

Plusieurs dizaines d’années se sont écoulées depuis les premières réparations de tétralogie de Fallot. On a pu espérer que les résultats immédiats, le plus souvent brillants, de ces réparations se maintiendraient définitivement et que les patients pourraient bénéficier d’une vie de durée et de qualité proches de la normale. C’est probablement cet espoir qui a justifié l’appellation de « cure complète » donnée depuis longtemps à cette opération, par opposition à la chirurgie palliative. Il faut malheureusement se rendre à l’évidence : de nombreux patients, même ceux qui ont bénéficié des techniques les plus raffinées de chirurgie et de protection myocardique, n’ont pas un cœur normal et risquent de souffrir de troubles variables dans leur délai d’apparition, leurs manifestations cliniques et leur gravité.
La surveillance de ces patients laisse souvent à désirer pour diverses raisons :
- ils se croient eux-mêmes guéris de toute affection cardiaque, puisqu’ils n’ont souvent aucun souvenir de leur opération, faite dans la petite enfance et qu’ils ont pendant longtemps été indemnes de tout symptôme ;
- parvenus à l’âge adulte, ils ne sont généralement plus surveillés par les cardiopédiatres et pas (ou mal) pris en charge par les cardiologues d’adultes jusqu’à ce qu’apparaissent des troubles sérieux. On assiste ainsi depuis quelques années au développement de cette pathologie, fruit des premières décennies de la chirurgie cardiaque, pathologie encore mal connue, donc mal surveillée et probablement mal traitée. Dans la prise en charge de ces patients, la chirurgie a une place importante. Ce chapitre a pour but d’en définir les indications et les modalités.
Les causes de lésions résiduelles après réparation chirurgicale
La réparation de la tétralogie a deux buts principaux : la fermeture de la communication interventriculaire (CIV) et la levée de l’obstacle entre le ventricule droit et les artères pulmonaires. Pour atteindre ces deux buts, le chirurgien doit avoir recours à une série de gestes qui, tous, peuvent être à l’origine de séquelles.
L’incision du cœur et la résection musculaire
Classiquement, les lésions cardiaques sont abordées par une incision ventriculaire droite, permettant de réséquer les bandelettes musculaires obstructives et de fermer la CIV. Dans les premières années de cette chirurgie, cette incision était de grande taille, pour donner au chirurgien le confort qu’imposaient une relative inexpérience et surtout l’absence de techniques efficaces de cardioplégie. Elle est actuellement beaucoup plus petite, limitée à la partie haute de l’infundibulum. Depuis la fin des années 80, on a même proposé de ne plus faire d’incision ventriculaire et de n’utiliser qu’un abord atrial, éventuellement complété par une incision du tronc pulmonaire. En fait, cette solution est très imparfaite pour au moins deux raisons :
- la levée de l’obstacle intraventriculaire exige dans la quasi totalité des cas une résection musculaire intraventriculaire, qui peut être au moins aussi agressive et donc délétère pour la fonction ventriculaire que l’incision épicardique ;
- un certain nombre de réparations exigent la section de l’anneau pulmonaire et une incision du haut de l’infundibulum pas beaucoup plus petite que celle qui permet de faire la totalité de la réparation. On n’a d’ailleurs jamais pu démontrer la supériorité de cet abord transatrial sur l’abord ventriculaire classique. Malheureusement, on doit admettre que la réparation de la tétralogie comporte nécessairement une agression du muscle ventriculaire droit, soit directement, par section ou résection, soit indirectement, par lésions d’artères coronaires traversant le muscle au niveau de ces sections musculaires.
La fermeture de la CIV
Elle se fait très généralement par un patch. Les séquelles possibles de ce geste sont liées à des lésions du tissu de conduction. Le bloc auriculo-ventriculaire complet est devenu rare. Plus souvent, c’est la branche droite qui est lésée, participant à la genèse d’un bloc de branche plus ou moins complet, l’autre facteur de ce bloc pouvant être la résection musculaire. Il semble que ce trouble de conduction, longtemps considéré comme banal, voire inévitable, est moins anodin qu’on ne le pensait. Il semble même être de mauvais pronostic lorsqu’il s’aggrave au fil du temps. Par ailleurs, il n’est pas rare qu’il persiste un shunt résiduel, de degré variable, qui peut constituer l’une des imperfections de la réparation.
Le traitement de la sténose valvulaire pulmonaire
Dans un grand nombre de cas (très diversement appréciés dans les publications), l’appareil valvulaire pulmonaire participe à l’obstacle à l’éjection du ventricule par deux mécanismes, souvent associés : l’hypoplasie de l’anneau et la malformation du tissu valvulaire. Le traitement du premier mécanisme est la section de l’anneau, celui du second la commissurotomie. Dans les deux cas, on crée une insuffisance pulmonaire, aujourd’hui de plus en plus souvent mise en cause dans la détérioration des résultats à distance.
L’agrandissement de la voie pulmonaire
Dans la très grande majorité des cas, la levée de l’obstacle pulmonaire nécessite l’agrandissement, par patch, de la voie d’éjection. Seules des formes anatomiques extrêmement favorables, à la limite de la définition stricte de la tétralogie, ne nécessitent pas d’agrandissement, au moins au niveau de l’infundibulum. En cas d’hypoplasie de l’anneau, ce patch est infundibulo-pulmonaire. S’il y a une sténose d’une branche pulmonaire ou des deux, il s’étend au-delà de la bifurcation. Les séquelles possibles de ce geste d’agrandissement sont de trois ordres :
- au niveau du ventricule, le patch est une zone akinétique, parfois dyskinétique dont l’existence même altère le fonctionnement ventriculaire ;
- sur l’ensemble de la voie d’éjection, il peut exister, immédiatement après l’opération ou plus tard, un ou plusieurs obstacles résiduels ;
- enfin, peuvent survenir des anévrismes soit par dilatation du tissu constituant le patch soit par distension du tissu naturel sur lequel a été fixé ce patch. Cette lésion est particulièrement fréquente au niveau de l’infundibulum du ventricule droit, et elle est souvent plus sévère du côté gauche du patch, sans doute parce que l’incision ventriculaire est responsable d’une interruption, de ce côté, de la perfusion venant de la coronaire droite.
À ces séquelles de la chirurgie, il faut ajouter les anomalies du lit vasculaire pulmonaire.
Leur sévérité, très variable, est très probablement dépendante des anomalies circulatoires fœtales accompagnant la cardiopathie. La diminution du flux pulmonaire peut empêcher la poursuite du développement pulmonaire après la naissance. Enfin, d’éventuelles interventions palliatives (anastomoses systémico-pulmonaires) peuvent aggraver les anomalies du lit pulmonaire par deux mécanismes : distorsions mécaniques et/ou sténose cicatricielle des artères sur lesquelles a porté l’anastomose, altérations du lit d’aval soit par hyperdébit, soit au contraire par mauvaise perfusion.
Indications chirurgicales
Les indications de la réintervention chirurgicale sont encore, malheureusement, très mal codifiées. Certes, il existe d’assez nombreuses publications concernant la réintervention sur tétralogie de Fallot. Elles concernent des patients qui ont en commun des symptômes quasi constants : limitation de la capacité d’effort, insuffisance pulmonaire, dilatation et/ou dysfonction ventriculaire droite, troubles du rythme. Cependant, ces différentes séries sont très peu homogènes quant à la sévérité de ces symptômes, le recul par rapport à la réparation initiale, l’âge de cette réparation. Il n’existe pas, à notre connaissance, de publications concernant des indications de réintervention dans des séries de patients suivis de façon prospective, étudiant l’évolution de cette symptomatologie ainsi que la qualité du lit vasculaire pulmonaire. Nous nous bornerons donc à énumérer les symptômes et les anomalies qui peuvent amener à discuter une réintervention.
Signes cliniques
Il s’agit de manifestations d’insuffisance cardiaque. La plus banale d’entre elles est la limitation des capacités d’effort physique. Cette gêne est souvent d’appréciation difficile car, de survenue progressive, elle est souvent minimisée par le patient. On ne devrait plus voir arriver à la chirurgie des patients qui ont tous les signes classiques de l’insuffisance cardiaque droite, ou même de l’insuffisance cardiaque globale, comme c’est encore trop souvent le cas.
Troubles du rythme
La survenue de troubles du rythme est très souvent le signal d’alarme qui, à la fois, amène le patient à consulter un cardiologue et constitue l’occasion de faire un bilan des lésions résiduelles. Ces troubles peuvent être très variables dans leur gravité : fibrillation, flutter ou tachysystolie auriculaires, extrasystolie, tachycardie voire épisodes de fibrillation ventriculaire. L’élargissement progressif du QRS est maintenant considéré comme un facteur pronostique permettant de prévoir l’augmentation du risque d’arythmies ventriculaires graves.
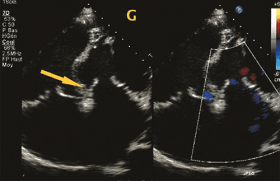
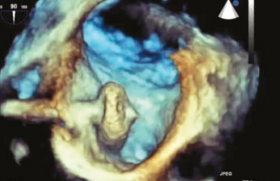
Dilatation et dysfonction ventriculaires droites, insuffisance valvulaire
C’est par l’échographie et, plus récemment, par la résonance magnétique que sont étudiées les anomalies ventriculaires et valvulaires. La dilatation ventriculaire droite est quasi constante chez les patients candidats à une réintervention. Elle s’accompagne fréquemment d’une altération plus ou moins sévère de la fonction systolique qui devrait être évaluée systématiquement chez tous les opérés. L’apparition ou l’aggravation d’une telle dysfonction est un élément important dans l’indication d’une réintervention. Il est en outre important d’analyser la part qui revient, dans la dilatation, à l’existence d’un anévrisme de la voie de sortie du ventricule droit. Bien que cette lésion ait fait l’objet de beaucoup moins d’études que les anévrismes ischémiques du ventricule gauche, il est difficile d’imaginer qu’elle n’ait pas les mêmes conséquences sur la fonction ventriculaire et sur la genèse de troubles du rythme ventriculaire. Nous pensons par conséquent qu’elle mérite une analyse préopératoire et un traitement chirurgical spécifiques.
L’insuffisance valvulaire pulmonaire est moins méconnue. Inévitablement associée aux réparations comportant une section de l’anneau et un patch infundibulo-pulmonaire, elle peut survenir après une simple commissurotomie, voire sans qu’aucun geste n’ait été fait sur la valve lors de la réparation : il s’agit alors, vraisemblablement, d’une dilatation de l’anneau liée celle du ventricule et à des imperfections de la réparation artérielle pulmonaire. Il s’agit donc à la fois d’une cause et d’une conséquence des anomalies qui sont à prendre en compte dans le traitement du patient ; il est illogique, comme on le voit malheureusement faire trop souvent, de n’analyser et de ne traiter que ce seul facteur au sein d’une pathologie à l’évidence plurifactorielle.
L’insuffisance tricuspide accompagne généralement la dilatation et la dysfonction ventriculaires droites. Elle peut être aggravée par des lésions organiques secondaires au geste initial de réparation : limitation de la mobilité du feuillet septal lors de la fixation du patch de CIV, lésion de l’appareil sous-valvulaire lors de la résection intraventriculaire. Lorsqu’elle est massive, cette insuffisance valvulaire doit faire l’objet d’un geste spécifique lors de la réintervention.
La dilatation et la dysfonction ventriculaires gauches ne sont pas exceptionnelles à un stade avancé de la maladie. Dans certains cas, en particulier chez des patients réparés tard dans la vie, après une ou plusieurs anastomoses palliatives, cette dégradation est au moins en partie due à une insuffisance aortique, elle-même en relation avec la dilatation aortique. Elle peut être favorisée par l’existence d’un shunt résiduel à l’étage ventriculaire. Parfois, cependant, aucun de ces mécanismes ne peut être mis en cause. Il est possible que la dysfonction gauche soit favorisée par deux mécanismes liés au ventricule droit. Le premier est l’anomalie de la géométrie et de la cinétique du septum interventriculaire ; le second pourrait être l’asynchronisme de contraction secondaire aux troubles conductifs intra-ventriculaires. Quoi qu’il en soit, il est important, dans l’étude préliminaire à la réintervention, d’étudier la fonction ventriculaire gauche. Il est trop facile d’incriminer la notion assez vague de séquelle d’une mauvaise protection myocardique.
Indications chirurgicales
Il n’est guère possible, dans l’état actuel de nos connaissances, de définir les indications précises à réintervenir chirurgicalement sur une tétralogie de Fallot. Il faut se résoudre à admettre les notions suivantes, généralement ignorées ou méconnues à la fois par les patients et par les cardiologues :
- ces patients ne sont presque jamais « complètement » réparés ;
- ils doivent être attentivement suivis, depuis la réparation jusqu’à la fin de leur vie par des médecins compétents dans ce domaine, alors que bien souvent ils sont abandonnés, à la fin de l’adolescence, par les cardiopédiatres pour être repris en charge, généralement trop tard, par des cardiologues peu intéressés par cette pathologie ou par des spécialistes d’un symptôme (trouble du rythme, insuffisance cardiaque, fuite valvulaire, etc.) qui ignorent plus ou moins consciemment la multiplicité des facteurs sur lesquels on peut et l’on doit intervenir.
Sans pouvoir disposer de critères objectifs précis, force est de discuter l’indication d’une réintervention sur des critères de bon sens :
- l’apparition ou l’aggravation de la gêne fonctionnelle,
- la nécessité d’un traitement médicamenteux,
- la survenue de troubles du rythme,
- l’aggravation de la dilatation ventriculaire et/ou l’altération de la fonction ventriculaire.
La réintervention chirurgicale
La réintervention sur tétralogie de Fallot préalablement réparée ne doit pas avoir comme objectif de traiter l’un des facteurs, même s’il est jugé primordial, des troubles dont souffre le patient. Le plus souvent, à la fois les cardiologues et les chirurgiens décident de « valvuler » la voie pulmonaire sans s’attacher aux autres anomalies qui peuvent déterminer l’avenir. Il est important d’agir sur tous les mécanismes qui peuvent participer à la genèse de ces troubles. Outre la correction des fuites valvulaires, la chirurgie doit viser à remodeler la voie pulmonaire, depuis le ventricule jusqu’aux branches, à traiter l’anévrisme, quasi constant, de l’infundibulum et à faire les gestes nécessaires à la prévention des troubles du rythme.
L’un des problèmes les plus difficiles, en pratique, est l’organisation de cette réintervention dans une structure adaptée. De nombreux centres de chirurgie cardiaque pédiatrique ne peuvent accueillir des patients adultes ; ils ne disposent pas du personnel médical, infirmier, technique requis, du matériel adapté et certains n’ont pas le droit de traiter des adultes. À l’opposé, la plupart des centres de chirurgie cardiaque d’adulte n’ont pas les compétences nécessaires pour analyser et traiter correctement ce type de patients : non seulement les chirurgiens mais les anesthésistes, les réanimateurs, les techniciens de CEC, les infirmières doivent posséder une expérience spécifique de la pathologie cardiaque congénitale pour que ces réinterventions, souvent techniquement difficiles, soient faites dans les conditions de qualité et de sécurité souhaitables.
Dans la très grande majorité des cas, l’intervention peut être faite en normothermie, sans clampage aortique et donc à cœur battant. Il y a deux exceptions à cette règle : l’existence d’un shunt résiduel, et la nécessité d’aborder l’oreillette gauche pour traiter des troubles du rythme. Il faut alors arrêter le cœur pendant le temps intracardiaque, en utilisant les techniques habituelles de cardioplégie (cardioplégie chaude intermittente pour les auteurs de cet article). Dans tous les cas, il est préférable de canuler les deux veines caves.
L’analyse préopératoire de la voie pulmonaire (par résonance magnétique et/ou scanner et/ou angiographie) guide le chirurgien pour le remodelage de la voie pulmonaire. Le principe en est simple : toutes les zones dilatées doivent être réduites, tous les obstacles résiduels doivent être levés.
Très généralement, on commence par ouvrir le patch d’agrandissement mis en place lors de la réparation. Ce patch est réséqué partiellement ou plus souvent totalement. S’il existe une sténose du tronc pulmonaire ou d’une branche, l’incision est prolongée au travers de la zone rétrécie jusqu’à la région où l’artère reprend un calibre normal. Cette zone sera agrandie lors de la mise en place du nouveau patch. Il peut y persister des obstacles distaux qui n’ont pas été traités lors de la réparation initiale, en particulier lorsqu’ont été faites des anastomoses palliatives. Ces lésions peuvent faire l’objet d’un traitement spécifique : abord de la branche pulmonaire intéressée et agrandissement par un patch distinct de celui qui sera utilisé sur la voie pulmonaire centrale. Lorsque l’abord chirurgical d’une des branches est difficile à cause des adhérences, il peut être plus facile et plus efficace de mettre en place un stent pendant l’opération, sous contrôle de la vue. Cette technique est rapide, ne demande aucun équipement particulier d’imagerie en salle d’opération et, lorsque la croissance corporelle est terminée, peut permettre d’espérer un bon résultat à long terme.
Dans la très grande majorité des cas, l’une des lésions justifiant la réintervention est l’insuffisance valvulaire pulmonaire. La mise en place d’une valve est l’une des phases importantes de la réintervention. Divers types de substituts peuvent être utilisés. Le plus classique est l’homogreffe, largement utilisée dans les pays anglo-saxons.
Ce substitut n’est cependant pas sans défaut : les résultats à long terme des conduits extracardiaques ne sont pas aussi brillants que ce que l’on avait pu espérer, quelle que soit la méthode de conservation (cryopréservation ou stérilisation par les antibiotiques). Il est possible que l’utilisation de ces homogreffes en position anatomique, c’est-à-dire placées dans la voie pulmonaire naturelle et non dans un conduit extracardiaque, en améliore la longévité. Cependant, ces imperfections, associées à la difficulté d’approvisionnement, ont justifié le recours à des xénogreffes, en général sans support armé. Les résultats varient suivant les publications mais la durabilité est en général un peu inférieure à celle des homogreffes. Notre expérience de ces substituts hétérologues non armés a été décevante. Qu’il s’agisse d’homogreffes ou de xénogreffes, il est possible qu’une part des échecs tienne à des facteurs mécaniques ; il est, en effet, difficile de mettre en place de telles valves dans des voies pulmonaires rendues rigides par les interventions antérieures, d’autant qu’il existe souvent une angulation naturelle entre la partie ventriculaire et la partie vasculaire de la voie pulmonaire. De plus, la valve, située dans une position très antérieure dans le thorax, est souvent comprimée par la paroi.
C’est pour remédier à ces facteurs mécaniques de dysfonctionnement que, comme d’autres groupes, nous utilisons actuellement, chez les patients de taille adulte, des prothèses péricardiques armées. Il faut savoir que, malgré leurs avantages, ces prothèses armées comportent le risque de compression du tronc de la coronaire gauche. Cette compression peut ne se manifester qu’à la fermeture du thorax. Ce risque doit être connu et, au moindre doute, il faut déplacer la prothèse pour éviter la compression coronaire ou la remplacer par une prothèse souple.
Chez des patients opérés à plusieurs reprises, il n’est pas illogique d’utiliser des prothèses mécaniques, malgré les inconvénients d’un traitement anticoagulant définitif. Les quelques résultats publiés à propos de cette technique sont encourageants.
Le traitement de la dilatation anévrismale de l’infundibulum, lésion quasi constante dans ces réinterventions, est une étape essentielle. Après l’ablation du patch ventriculaire mis en place lors de la réparation, on voit de façon quasi constante, sur les berges ventriculaires auxquelles ce patch était suturé, une zone plus ou moins large de tissu aminci, fibreux, souvent plus développée du côté gauche de l’infundibulum. Certains auteurs ont proposé de plicaturer ce tissu fibreux pour réduire la taille de la cavité à ce niveau. Nous préférons utiliser une technique fondée sur les principes de celle que Dor et coll. utilisent avec succès depuis de nombreuses années pour les anévrismes ischémiques du ventricule gauche : elle consiste à remodeler, par un patch endoventriculaire, la zone anévrismale en donnant à cette partie du ventricule les dimensions et la forme souhaitées, ce patch étant dans tous les cas suturé en zone musculaire saine et non pas sur le tissu fibreux. Suivant également le principe appliqué avec succès par Dor et coll. pour le traitement et la prévention des troubles du rythme ventriculaire, nous faisons systématiquement une cryoablation de la zone de jonction entre le tissu fibreux anévrismal et la zone musculaire saine. Il est, en effet, hautement vraisemblable que ce soit cette zone qui soit à l’origine des arythmies ventriculaires. Le geste de cryoablation est rapide, son risque est minime et nous paraît en tout cas justifié par celui de la récidive ou de l’apparition de novo de tachycardie ventriculaire après la réintervention.
Chez les patients souffrant de troubles du rythme auriculaire (flutter ou fibrillation), il peut être indiqué de faire un geste d’ablation auriculaire. Les lignes de cryoablation, pour ces arythmies prenant vraisemblablement leur origine dans l’oreillette droite, sont moins bien définies que dans les indications habituelles. Outre les lignes classiques d’ablation de l’oreillette gauche, nous faisons plusieurs lignes d’ablation dans l’oreillette droite : une première ligne va de la partie droite de l’orifice du sinus coronaire au bord gauche de l’orifice de la veine cave inférieure ; une seconde joint la première à la tricuspide; une troisième relie la fosse ovale au toit de l’oreillette, à gauche de l’orifice cave supérieur ; une quatrième, enfin, relie la fosse ovale à l’atriotomie située en avant, parallèle au sillon auriculo-ventriculaire droit.
Quelle intervention ?
La réintervention typique sur tétralogie de Fallot comprend donc les étapes suivantes :
- résection de l’ancien patch et éventuelle incision des sténoses du tronc et des branches de l’artère pulmonaire ;
- mise en place, au niveau de la jonction entre ventricule et tronc pulmonaire, d’une prothèse valvulaire armée ;
- cryoablation des berges de l’anévrisme ventriculaire ;
- mise en place d’un patch infundibulo-pulmonaire. La partie haute, artérielle, de ce patch est taillée de manière à donner un calibre harmonieux au tronc et à la bifurcation. Au niveau de la prothèse valvulaire, sa largeur est mesurée pour venir recouvrir la portion d’anneau qui n’a pas été suturée aux tissus naturels. Au niveau du ventricule, ce patch, taillé de manière à donner à la voie de sortie un calibre normal, est fixé à l’intérieur du ventricule aux berges saines, musculaires, de l’infundibulum.
En pratique
Rares sont les tétralogies de Fallot qui peuvent être considérées comme guéries après réparation ; il faut définitivement supprimer du langage médical courant, pour cette malformation, le terme de « cure complète ». Tous les patients doivent être suivis par des cardiologues particulièrement compétents dans le domaine des affections congénitales, même et surtout lorsqu’ils sont devenus adultes.
Beaucoup d’entre eux nécessiteront, au cours de leur vie, de nouveaux traitements, parmi lesquels la chirurgie garde malheureusement une place importante. Ces réinterventions doivent, comme la surveillance médicale, être faites par des équipes spécialisées. Elles comportent en général plusieurs gestes visant à corriger toutes les anomalies résiduelles responsables de la symptomatologie du patient.
Bien des progrès restent à faire dans l’approche médico-chirurgicale de ces patients, qui seront, dans les années à venir, de plus en plus nombreux.
Attention, pour des raisons réglementaires ce site est réservé aux professionnels de santé.
pour voir la suite, inscrivez-vous gratuitement.
Si vous êtes déjà inscrit,
connectez vous :
Si vous n'êtes pas encore inscrit au site,
inscrivez-vous gratuitement :