Publié le 15 nov 2011Lecture 14 min
Utilisation des HBPM chez le sujet âgé insuffisant rénal
J.-F. ALEXANDRA, Hôpital Bichat, Paris
Le risque d’accumulation des HBPM en cas d’insuffisance rénale est pratiquement la seule limite à l’utilisation de ces molécules. Cette situation est d’autant plus gênante que le risque de survenue d’une TVP est accru en cas d’insuffisance rénale associée à une albuminurie supérieure à 30 mg/jour(1).
HBPM et fonction rénale altérée
Le risque d’accumulation des HBPM en cas d’insuffisance rénale est pratiquement la seule limite à l’utilisation de ces molécules. Cette situation est d’autant plus gênante que le risque de survenue d’une TVP est accru en cas d’insuffisance rénale associée à une albuminurie supérieure à 30 mg/jour(1). Jusqu’à 52 % des patients avec une TVP ont ainsi une insuffisance rénale légère à modérée(2).
La prescription d’HBPM chez l’insuffisant rénal implique un certain nombre de précautions. En premier lieu, il importe de mesurer avec le plus de fiabilité possible le débit de filtration glomérulaire (DFG). Ce point sera particulièrement sensible chez le sujet âgé. Nous y reviendrons largement alors, mais notons déjà que les poids extrêmes, la dénutrition, etc. sont des circonstances où même chez l’adulte jeune, les méthodes indirectes d’estimation du DFG peuvent être prises en défaut.
Cette évaluation est une nécessité rappelée par l’Afssaps :
« En cas d’insuffisance rénale sévère définie par une clairance de la créatinine inférieure à une valeur de l’ordre de 30 ml/min, il existe une contre-indication de l’utilisation des HBPM à dose curative et des précautions d’emploi lors de leur utilisation à dose préventive. Si les HBPM sont contre-indiquées, l’HNF peut être utilisée.
En cas d’insuffisance rénale modérée (clairance de la créatinine comprise entre 30 et 60 ml/min), il existe des précautions d’emploi pour l’utilisation des HBPM à dose curative. Dans tous les cas, l’évaluation de la fonction rénale par la formule de Cockcroft doit être systématique après 75 ans (http://www.afssaps.sante.fr) ».
La principale et historique alternative aux HBPM est l’héparine non fractionnée (HNF) qui est éliminée par le système réticulo-endothélial mais nécessite une surveillance biologique quotidienne et un abord veineux préférentiel rendant son usage lourd, imposant une surveillance hospitalière. L’obtention de données claires quant à l’usage des HBPM chez l’insuffisant rénal est donc un enjeu important pour une situation clinique fréquente.
Comment estimer la fonction rénale ?
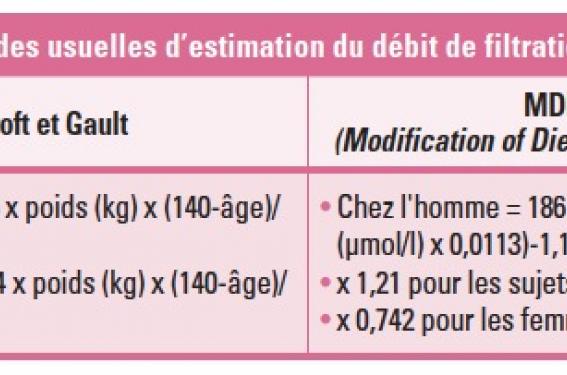
Répondre à cette question signifierait être capable de déterminer le DFG de manière fiable pour tous les sujets. Malheureusement, les estimations par les formules de Cockcroft et Gault ou par le MDRD sont imparfaites (tableau 1).
Ces deux formules sous-estimeraient le DFG r.el de respectivement 25 % et 10 % au-delà de 65 ans. Les données manquent en réalité dans le grand âge(3), population dans laquelle la prévalence d’une insuffisance rénale modérée (stade 3 [tableau 2]) est élevée. On ne peut en aucun cas se baser sur le seul chiffre de créatinine, reflet d’une masse musculaire pouvant beaucoup varier dans les âges extrêmes.
Globalement, ces méthodes indirectes de mesure ne permettent de classer correctement que 2/3 des patients âgés en regard de leur degré d’insuffisance rénale(4). Pour les autres, en cas de traitement néphrotoxique ou à élimination rénale, la question d’autres méthodes de mesure doit se poser (cystatine C en cours d’évaluation, mesure au laboratoire d’explorations fonctionnelles, etc.).
Si l’on s’en tient aux études épidémiologiques, la diminution du DFG est estimée à 1 % par an au-delà de 40 ans, mais les écarts interindividuels sont majeurs. On considère qu’environ 50 % des plus de 70 ans ont un DFG < 60 ml/min/1,73 m2(5), ce qui est résumé dans le tableau 3.
La prévalence d’une insuffisance rénale chronique et l’impossibilité de l’estimer par la seule valeur de la créatinine plasmatique imposent un calcul du DFG chez tous les patients âgés. En cas de doute (poids extrême, sarcopénie importante, etc.) ou de traitement prolongé à élimination rénale, des méthodes de mesure plus précises que les formules usuelles peuvent être discutées.
Qu’est-ce qu’une HBPM ?
Pour commencer, il faut revenir à la molécule d’héparine elle-même d’où proviennent les différentes HBPM. L’héparine est composée de différentes chaînes polysaccharidiques de poids moléculaire (PM) allant de 3 000 à 30 000 daltons mais surtout compris entre 13 000 et 15 000 daltons. L’activité anticoagulante est liée aux chaînes d’héparine porteuses d’un pentasaccharide (1/3), qui permet la liaison à l’antithrombine, inhibant autant le facteur Xa que la thrombine (le rapport anti-Xa/anti-IIa de l’HNF est égal à 1) pendant que les 2/3 restants des chaînes n’ont pas d’effet anticoagulant. Différentes techniques immunoenzymatiques permettent de couper la chaîne d’HNF pour obtenir les HBPM dont le poids moléculaire varie de l’une à l’autre. Ces différences semblent ne pas influencer l’effet anticoagulant de ces molécules, la coupure conservant les capacités d’inhibition du facteur Xa, mais l’inhibition de la thrombine sera plus marquée avec les chaînes les plus longues.
En revanche, la clairance rénale des HBPM sera modifiée par le poids moléculaire (PM) : plus le PM diminue, plus la voie d’élimination des HBPM sera rénale, les HBPM plus lourdes étant également métabolisées par le système réticulo-endothélial, profil d’élimination plus proche de l’HNF(6). Le poids moléculaire le plus élevé est celui de la tinzaparine (6 500 Da), puis la daltéparine et la nadroparine (5 800 Da) et l’énoxaparine (4 500 Da)(7).
Clairance rénale des différentes HBPM
De plus en plus de données amènent donc à considérer que le profil d’élimination rénale varie d’une HBPM à l’autre. Cependant, peu de comparaisons entre les molécules sont disponibles et les études souffrent de l’hétérogénéité des patients recrutés et d’un caractère volontiers rétrospectif. Nous examinerons les 4 HBPM disponibles en France pour lesquelles les données sont les plus étayées dans la littérature.
Énoxaparine : c’est l’HBPM la mieux étudiée. Son faible poids moléculaire la rend très sensible aux variations de la créatinine plasmatique : une augmentation de 20 μmol/l pourrait ainsi majorer de 40 % le risque hémorragique(8). Il existe une forte corrélation entre le DFG et l’accumulation d’énoxaparine mesurée par l’activité anti-Xa(9), y compris à dose prophylactique(10). Cette corrélation est pertinente cliniquement : aux doses curatives, le risque de complication hémorragique est majoré si le DFG est < 30 ml/min passant de 2,4 à 8,3 %(11). L’adaptation des doses à l’activité anti-Xa pourrait diminuer ce surrisque(11), mais aucune étude ne valide actuellement cette attitude. À dose préventive, on retrouve une augmentation progressive de l’activité anti-Xa si le DFG est < 30 ml/min(12), mais le surcroît de risque hémorragique est moins bien démontré(13).
Daltéparine : les données sont beaucoup plus rares. Dans une étude prospective portant sur des patients dialysés, aucune accumulation de daltéparine n’est retrouvée quand elle est administrée à dose préventive. Il n’y a pas de données à doses curatives(14).
Nadroparine : il n’y a pas de données à large échelle concernant cette molécule, mais il paraît exister une accumulation dès le stade d’insuffisance rénale modérée par rapport au volontaire sain(15).
Tinzaparine : la clairance de la tinzaparine est peu modifiée après une dose unique chez l’insuffisant rénal chronique(16). Ce résultat est attendu compte tenu du PM de la molécule. Il est confirmé par plusieurs autres études ne retrouvant pas de corrélation entre le DFG et l’activité anti-Xa chez les patients sous tinzaparine utilisée à dose préventive ou curative(10). Cependant, une réduction empirique de dose était parfois réalisée et les seuls surdosages rapportés se sont produits en cas de DFG < 30 ml/min, seuil qui réduit la clairance de la tinzaparine d’environ 24 %(17). Aucune conclusion définitive ne peut donc être tirée. Même si le risque d’accumulation paraît minoré par rapport aux autres HBPM, il ne semble pas nul pour autant.
Le risque d’accumulation des HBPM est clairement dépendant de la fonction rénale et du type de molécule choisi. La relation linéaire entre DFG et activité anti-Xa n’existe pas pour toutes les molécules. Il n’y a donc pas de base scientifique forte pour imposer une fourchette basse à l’administration de l’ensemble des HBPM(18), mais un certain nombre de précautions de bon sens rejoignant partiellement les recommandations de l’Afssaps.
Rapport bénéfice-risque du traitement anticoagulant en gériatrie
Le risque hémorragique lié au traitement anticoagulant est estimé autour de 3,8 % par an avec une mortalité de l’ordre de 20 %, ce qui est à contrebalancer par une mortalité nettement supérieure chez les patients non traités par MVTE. L’EP massive est en effet responsable de 4 à 8 % de la mortalité en milieu hospitalier(19) et est incriminée dans les séries autopsiques dans 4 à 11 % des décès dont les trois quarts concernent des patients issus de service de médecine(20). La mortalité hospitalière de la maladie veineuse thromboembolique est évaluée à 12 %(21).
L’âge est communément admis comme procurant un surcroît de risque hémorragique et est intégré dans les scores de risque (cf. infra). Pourtant, cette notion est fortement contredite, d’une part par le caractère très hétérogène de la population âgée qui cumule différents facteurs de risque de saignement (polymédication en particulier antithrombotique, insuffisance rénale mésestimée par une créatinine faussement rassurante, etc.), d’autre part, par des études récentes. Ces dernières ne retrouvent pas d’excès de saignement lié à l’âge tant dans une métaanalyse(22) que dans un essai prospectif mené avec la tinzaparine ajustée au poids et à l’activité anti-Xa(23). Le risque de saignement majeur dans ce dernier essai est de l’ordre de 1,5 %, ce qui n’est pas différent des données de la littérature alors qu’il s’agissait d’une population très âgée (moyenne d’âge de 85 ans). Une autre étude observationnelle estime à 7 % l’incidence de saignements majeurs et mineurs chez les sujets âgés, phénomène majoré par l’insuffisance rénale(24). Les saignements sont volontiers rapportés en cas de co-prescription des HBPM à d’autres molécules anticoagulantes et généralement sans surdosage retrouvé(25). Le grand âge n’est donc pas de manière formelle un facteur indépendant de risque hémorragique.
Le type de traitement n’apparaît pas clairement non plus comme variable discriminante : il n’y a pas de preuve solide démontrant une moindre incidence de saignement sous HNF que sous HBPM. Dans la récente étude prospective IRIS, il n’y a pas plus de risque hémorragique chez le sujet âgé traité par tinzaparine que par HNF, même en cas d’insuffisance rénale(26).
Les études plus anciennes font plutôt état d’un risque similaire, majoré par l’insuffisance rénale dès que le DFG est < 60 ml/min(27). On ne retrouve aucune étude démontrant formellement un usage plus sûr de l’HNF comparativement aux HBPM.
De plus, si la corrélation de l’âge au risque hémorragique n’est pas démontrée avec les HBPM, elle l’est en revanche avec l’HNF !(28)
Contrairement aux idées reçues, les chutes ne sont pas un facteur de risque de saignement bien que les hémorragies les plus graves compliquent souvent un traumatisme.
L’enjeu reste cependant d’identifier les patients les plus à risque de complication hémorragique. À cette fin, Ruiz-Gimenez a proposé en 2008 le score de RIETE pouvant aider à la décision (tableau 5).
En fonction de ce score, un risque de saignement annuel peut être estimé (tableau 6).
À ce score, viennent s’ajouter les facteurs de risque plus « traditionnels » : antécédent d’hémorragie digestive, accident vasculaire cérébral, alcoolisme, diabète, association à des antiagrégants, premiers jours de traitement, etc.
Bien qu’intégré à ce score, on voit que l’âge n’est sans doute pas un facteur de risque univoque.
Par ailleurs, les doné.es de l’enquête Afssaps 2001 ont montré que la plupart des complications hémorragiques sévères étaient liées :
– à l’insuffisance rénale ;
– aux traitements prolongés au-delà de la durée usuelle préconisée de 10 jours ;
– aux non-respects des modalités thérapeutiques conseillées (schéma posologique, surdosage, utilisation hors AMM).
Comment utiliser ces données en pratique ? On voit que les éléments les plus pertinents pointent un risque hémorragique anticipable : saignement récent, anémie, antécédent d’hémorragie massive, insuffisance rénale, prescription conjointe d’AVK dans le cadre du relais, co-prescription d’antiagrégant plaquettaire… qui en font une sous-population à risque élevé mais facile à identifier.
C’est alors au contrôle de ces éléments (différer le traitement à la résolution du saignement, poser clairement l’indication d’une prescription d’antiagrégant plaquettaire, surveiller très étroitement l’INR à l’introduction du traitement, identifier dans une population âgée celle dont le DFG est altéré) et à la prévention de tout mésusage plus encore qu’au traitement par HBPM lui-même qu’il faudra accorder toute son importance.
Ces facteurs de risque clairement identifiables et potentiellement réversibles sont une des clés pour minimiser le risque de complications, dans une population âgée qui n’est pas plus à risque du seul fait de l’âge, mais où la fréquence de la MVTE impose une bonne connaissance du maniement des anticoagulants.
Prescription d’une HBPM chez le sujet âgé avec une fonction rénale « conservée »
L’âge n’étant pas un obstacle en soi à l’usage des HBPM, la question de leur emploi en gériatrie est-elle incongrue pour autant ?
La réponse est naturellement triviale : non. Mais les raisons qui amènent à reconnaître une spécificité au sujet âgé sont multiples :
– polymédication avec nombreux traitements modifiant l’hémostase (antiagrégants plaquettaires, autres anticoagulants, molécules altérant la fonction rénale, etc.) ;
– fréquence de l’insuffisance rénale ;
– fréquence des comorbidités.
Les données de la littérature sont parcellaires, les sujets âgés étant volontiers exclus des essais cliniques et les essais spécifiques à la gériatrie entravés par la fréquence des troubles cognitifs empêchant les patients hospitalisés de donner un consentement éclairé. En l’absence d’insuffisance rénale, les recommandations des HBPM à visée prophylactique semblent pouvoir s’appliquer aux sujets âgés même si quelques données évoquent une possible accumulation de l’énoxaparine à dose préventive chez le sujet âgé(29) qui n’est retrouvée ni avec la tinzaparine ni avec la nadroparine(18). La prudence est surtout recommandée pour les posologies curatives.
De nombreuses stratégies visant à minimiser le risque hémorragique quoique mal étudiées sont très répandues : 96 % de 207 hôpitaux interrogés aux États-Unis, Angleterre, Nouvelle-Zélande et Australie déclaraient récemment modifier la posologie des HBPM chez les sujets âgés en fonction de critères tels que le poids, la fonction rénale ou l’activité anti-Xa(30).
Chez le sujet âgé normo-rénal, la principale stratégie est la mesure de l’activité anti-Xa. Le rationnel est d’anticiper un surdosage ou une accumulation. En effet, de hauts niveaux d’anti-Xa sont associés à un risque hémorragique accru(25). Cette attitude est d’autant plus logique que l’intervalle thérapeutique est bien connu, même s’il est variable selon l’HBPM utilisée (cf. tableau de Boneu) et qu’une activité anti-Xa au-delà de la borne supérieure est aisée à repérer.
Dans une étude prospective menée avec la tinzaparine, environ 10 % des patients qui recevaient une dose curative fixe de 175 UI/kg avaient une activité anti-Xa trop élevée, sans corrélation avec le DFG. Ils ont bénéficié d’une réduction de dose(23), sans que cette attitude entraîne d’augmentation des complications thrombotiques. Ce monitorage semble ainsi une attitude sûre, d’autant que le surdosage est difficilement anticipable. Cependant, cette attitude, validée avec la tinzaparine, ne peut être généralisée à toutes les HBPM qui ne sont pas équivalentes en termes d’élimination rénale et d’objectif d’activité anti-Xa(31). Ce d’autant qu’une réduction trop drastique expose à une perte d’efficacité du traitement(32). La sécurité d’une réduction de dose et ses modalités doivent donc être évaluées de manière prospective pour chacune d’entre elles.
On peut tout de même énoncer un certain nombre de règles de bonnes pratiques communément admises :
• Respecter les schémas posologiques de chaque HBPM en recueillant un poids récent mesuré et non estimé.
• Estimer systématiquement la fonction rénale (cf. infra).
• Ne pas utiliser d’HBPM à dose curative en dessous d’un DFG < 30 ml/min. Monitorer alors l’activité anti-Xa pour les doses préventives.
• Mesurer l’activité anti-Xa peut être utile si le DFG est entre 30 et 60 ml/min (insuffisance rénale modérée) ou en cas de poids extrêmes (< 40 kg ou > 100 kg).
• Discuter en cas d’insuffisance rénale modérée une réduction de dose basée sur la mesure de l’anti-Xa 4 heures après la 3e injection en sachant que : en premier lieu, une réduction trop importante expose à une protection moindre et que, en second lieu, l’effet anti-Xa optimal est mal connu et variable selon la molécule employée.
• Privilégier les molécules dont l’accumulation en cas d’insuffisance rénale est moindre en sachant qu’elle n’est sans doute pas nulle.
• Respecter les modalités d’administration et de surveillance selon les recommandations récentes de l’Afssaps.
• Respecter les durées de traitement (10 jours à dose curative en dehors du patient atteint de cancer) et le cas échéant, débuter les AVK le plus précocement
possible.
• Éviter les associations médicamenteuses (anti-inflammatoires non stéroïdiens, antiagrégants plaquettaires, etc.). Chez le sujet coronarien ou polyvasculaire, il est impératif de bien peser l’association d’un anticoagulant à l’aspirine qui est souvent non indiquée.
Malgré l’absence d’étude à grande échelle, l’usage des HBPM chez le sujet âgé sans dysfonction rénale appelle un certain nombre de précautions. La généralisation du monitorage de l’activité anti-Xa est une stratégie qui demande à être plus largement validée et qui devra l’être individuellement pour chaque HBPM, les caractéristiques des unes n’étant pas extrapolables aux autres. Si les posologies curatives imposent la vigilance, on ne peut totalement exclure l’accumulation de certaines HBPM dès les doses prophylactiques.
Prescription d’une HBPM chez le sujet âgé insuffisant rénal chronique
C’est la situation qui cumule a priori le plus d’obstacles à la prescription d’une HBPM, que l’indication soit curative ou prophylactique. Au-delà de cette affirmation de principe, se dégage une réalité beaucoup plus floue et probablement moins uniforme qu’il n’y paraît. Nous avons déjà largement passé en revue les particularités des HBPM en cas de fonction rénale altérée et chez le sujet âgé. La conjonction de ces deux facteurs, fréquente (au moins 50 %) a fait naître une littérature spécifique résumée dans les tableaux 7 et 8.
Malgré une contre-indication formelle de l’Afssaps, les insuffisants rénaux traités par HBPM de manière curative n’ont pas nécessairement de surdosage biologique ni de surcroît franc de risque hémorragique. Si la tinzaparine offre sans doute un profil de sécurité particulier dans cette situation du fait de son poids moléculaire, il n’y a pas de preuve formelle de dangerosité des autres HBPM par rapport à l’HNF en cas d’insuffisance rénale.
De plus amples études sont nécessaires pour établir l’innocuité réelle (tant sur le plan hémorragique que thrombotique) et dicter des recommandations pour adapter finement les posologies de chaque HBPM à l’activité anti-Xa.
"Publié dans un supplément de Gérontologie Pratique"
Attention, pour des raisons réglementaires ce site est réservé aux professionnels de santé.
pour voir la suite, inscrivez-vous gratuitement.
Si vous êtes déjà inscrit,
connectez vous :
Si vous n'êtes pas encore inscrit au site,
inscrivez-vous gratuitement :