Trucs et astuces
Publié le 28 fév 2015Lecture 6 min
Pistes à explorer face à un patient non répondeur à la resynchronisation
C. ALONSO, CMC Ambroise Paré, Neuilly-sur-Seine
Vingt ans après la première publication sur la resynchronisation cardiaque (CRT) et plus de 10 ans après sa validation par une étude randomisée, nous observons encore environ un tiers de non-répondeurs à ce traitement(1, 2).
De quoi parle-t-on exactement lorsque l’on dit d’un patient qu’il est non répondeur ? Les études sur le sujet utilisent soit des critères cliniques (morbimortalité, qualité de vie, classe NYHA, etc.), soit des critères échographiques (volumes ventriculaires gauches, FEVG, etc.), soit encore une combinaison des deux, cette dernière approche semblant être la plus judicieuse. En effet, selon G.B. Bleeker et al., 27 % des répondeurs sur des critères cliniques sont non répondeurs sur des critères échographiques et 21 % des répondeurs sur des critères échographiques ne sont pas répondeurs sur des critères cliniques(3).
Quoi qu’il en soit, nous allons voir que la « non-réponse » à la CRT n’est pas une fatalité !
Classiquement, on doit se poser 3 questions face à un patient non répondeur :
• Était-il un bon candidat à la resynchronisation ?
• Est-il vraiment resynchronisé ?
• La prise en charge globale estelle optimale ?
Bon candidat ou non ?
Cette première question est sans doute la plus importante car si le patient n’est pas un bon candidat, on aura beau s’acharner, ça ne marchera pas. Dans la série de W. Mullens qui s’est intéressé aux non-répondeurs, 9 % des patients avaient un QRS spontané < 130 ms(4).
Nous ne manquons pourtant pas d’études montrant que la CRT est inefficace chez les patients ayant des QRS fins et ce même en présence de critères échographiques d’asynchronisme. Par ailleurs, la présence de pathologies associées nécessitant un traitement spécifique (coronaropathie justifiant une revascularisation, valvulopathie nécessitant une correction chirurgicale, etc.) ou de comorbidités (insuffisance respiratoire, insuffisance rénale, etc.) vont atténuer les bénéfices de la CRT même si le patient semble avoir par ailleurs une bonne indication de resynchronisation. La présence de tissu cicatriciel étendu est également à prendre en compte : « dead meat doesn’t beat » !
Le patient est-il resynchronisé ?
Mais c’est en se posant la seconde question que l’on va pouvoir bien souvent redresser la situation ; mon patient est- il vraiment resynchronisé, la thérapie est-elle délivrée ?
D’après B.P. Knight et al., on observe une perte de resynchronisation chez 36 % des patients au cours du suivi et celle-ci pourra être corrigée dans plus de 87 % des cas(5). Les causes les plus fréquentes sont les arythmies atriales et ventriculaires, les pertes de capture VD ou VG, ou une surdétection. Une programmation inadéquate (fréquence maximale trop basse, délai AV trop long, etc.) peut également conduire à un taux de stimulation biventriculaire (BiV) insuffisant. Un pourcentage de stimulation BiV < 90 % serait ainsi observé chez près d’un quart des non-répondeurs(4). Ces problèmes peuvent être évidents dès l’interrogation de l’appareil ou plus difficiles à détecter. Dans ce cas, le Holter et l’épreuve d’effort peuvent être d’un grand secours.
La figure 1 montre l’exemple d’un patient présentant une perte de capture VG intermittente. Le seuil de stimulation VG au repos était tout à fait correct et la perte de capture n’a été démasquée qu’à l’épreuve d’effort. Dans l’exemple de la figure 2, il s’agit d’une patiente restant très symptomatique malgré la resynchronisation. Le contrôle de l’appareil retrouve des paramètres électriques normaux sur les 3 sondes et aucune anomalie ne nous saute aux yeux. C’est finalement le Holter qui révèle un dysfonctionnement pouvant faire évoquer un défaut de détection de l’onde P. Il s’agissait en fait d’une surdétection intermittente de l’onde T.
Figure 1. Capture biventriculaire effective au repos (tracé de gauche), mais perte de capture VG lors de l’effort (tracé de droite) avec QRS élargis.
Figure 2. Holter ECG révélant un dysfonctionnement pouvant faire évoquer un défaut de détection de l’onde P. Il s’agit en fait d’une surdétection intermittente de l’onde T.
Bien que les études sur l’intérêt de l’optimisation du délai AV par différentes méthodes n’aient pas été concluantes, il faut néanmoins s’y intéresser chez les non-répondeurs. Dans la série de W. Mullens, on retrouve une programmation non optimale du délai AV responsable d’une altération du remplissage VG chez 47 % des non-répondeurs(4). Dans une sous-analyse de MADIT-CRT, la programmation d’un délai AV court (< 120 ms) est associée à un bénéfice clinique et échographique supérieur(6).
La qualité de la resynchronisation va bien évidemment dépendre de la qualité de l’implantation. Classiquement, la cible est la paroi latérale du VG car c’est celle dont la contraction est le plus souvent retardée, et l’on doit éviter les positions antérieures. D’après les sous-analyses de REVERSE et MADIT-CRT, il faut également éviter la position apicale pour la sonde VG. Pour W. Mullens, la position de la sonde VG était inadéquate chez 21 % des patients et chez 16 % des patients il persistait un asynchronisme mécanique malgré la stimulation BiV(4).
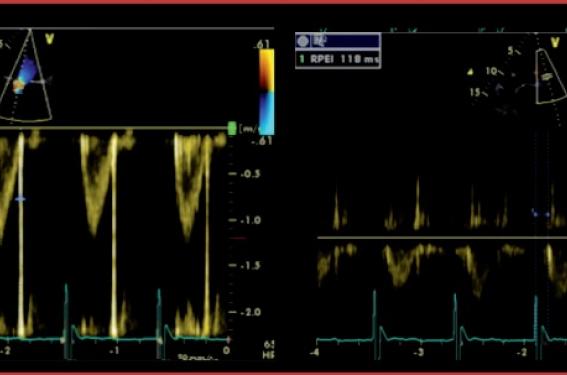
Mais le problème est plus complexe, et la qualité de la resynchronisation dépend en fait des positions relatives des sondes VD et VG. Bien sûr, cela est difficile à schématiser compte tenu des multiples combinaisons possibles et, dans les grandes études randomisées, la majorité des sondes VD étaient positionnées à l’apex. Certains ont suggéré que les sondes VD et VG devaient être éloignées anatomiquement, d’autres qu’il fallait enregistrer un délai aussi long que possible entre les signaux électriques enregistrés respectivement par les deux sondes. La figure 3 montre un exemple de l’influence de la position de la sonde VD sur la qualité de la resynchronisation ; la sonde VG étant dans une veine latérale, la sonde VD est d’abord placée sur le septum moyen (figure 3A), avec un délai pré-éjectionnel gauche à 192 ms et un délai pré-éjectionnel droit à 133 ms. La sonde VD est déplacée sur le septum haut (figure 3B), et le délai pré-éjectionnel gauche passe alors à 126 ms et le délai pré-éjectionnel droit à 118 ms, traduisant une meilleure resynchronisation.
Figure 3. Influence de la position de la sonde VD sur la qualité de la resynchronisation. La sonde VG étant dans une veine latérale, la sonde VD est sur le septum moyen (A), avec un délai pré-éjectionnel gauche à 192 ms et droit à 133 ms. La sonde VD est replacée sur le septum haut (B) et le délai pré-éjectionnel gauche passe à 126 ms et le droit à 118 ms, soit une meilleure resynchronisation.
La prise en charge globale
Enfin, il ne faut pas oublier la prise en charge globale de l’insuffisance cardiaque : le traitement médical non optimal, le non-respect des règles hygiénodiététiques, la présence d’une anémie sont autant de facteurs pouvant limiter les bénéfices de la CRT. Près d’un quart des patients n’aurait pas un traitement médical optimal, 30 % une anémie significative et 41 % un surpoids(4). Enfin, certains patients sont déconditionnés ce qui peut atténuer les bénéfices de la CRT. La réadaptation cardiaque devrait donc être recommandée à la plupart des patients.
Conclusion
Il ne faut pas baisser les bras face à un patient non répondeur. Une cause que l’on peut corriger peut être retrouvée chez ¾ d’entre eux.
Il faut la rechercher par des examens simples (bilan clinique et biologique, ECG, radio de thorax, contrôle de l’appareil, Holter et épreuve d’effort) et enlever nos œillères de rythmologue pour considérer la prise en charge globale de notre patient insuffisant cardiaque.
Attention, pour des raisons réglementaires ce site est réservé aux professionnels de santé.
pour voir la suite, inscrivez-vous gratuitement.
Si vous êtes déjà inscrit,
connectez vous :
Si vous n'êtes pas encore inscrit au site,
inscrivez-vous gratuitement :


