Complication
Publié le 28 fév 2015Lecture 6 min
Quand implanter un stimulateur cardiaque après un TAVI ?
F. SALERNO, J. HORVILLEUR, J. LACOTTE, M. AIT SAID, unité de rythmologie, Institut Cardiovasculaire Paris Sud, Massy
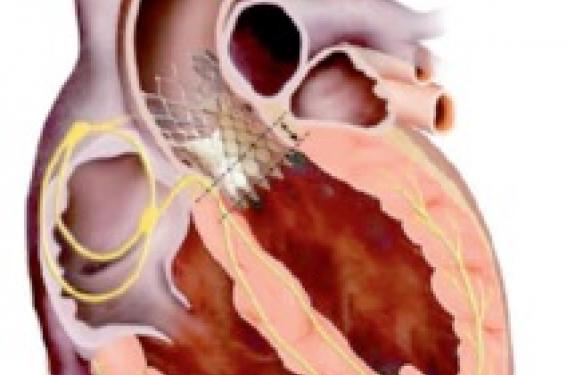
Alors que l’implantation de valve aortique par cathéter (TAVI) est devenue le traitement de prédilection des rétrécissements aortiques (RA) serrés à haut risque chirurgical, les indications devraient prochainement s’élargir aux patients avec risques intermédiaires. En post-TAVI, le taux d’implantation de stimulateurs (PM) est de l’ordre de 30 %. La question « Quand implanter un PM en post-TAVI ? » est donc plus que d’actualité.
Mécanisme des troubles conductifs
La branche gauche du faisceau de His prend son origine environ 6 mm en dessous de l’anneau aortique. Par ce rapport étroit, on comprend que les lésions de cette portion anatomique ne soient pas exceptionnelles au cours d’un TAVI. Elles sont induites par un traumatisme mécanique causant œdème et nécrose au niveau du septum membraneux durant les différentes étapes de la procédure : passage du guide dans la valve, prédilatation au ballon, déploiement de la valve, postdilatation au ballon(1).
La prothèse CoreValve® (Medtronic) – valve montée dans une cage auto-expansible – procure une force radiale continue au niveau de la chambre de chasse du ventricule gauche en regard de la branche gauche, créant ainsi une lésion tissulaire par compression importante de l’anneau calcifié sur le tissu adjacent(2).
La prothèse, Edwards Sapien® – valve disposée sur un stent –, dont le déploiement requiert une inflation à l’aide d’un ballon s’implante en position intra-annulaire(2). Les valves Edwards® exercent une action temporaire sur la branche gauche s’assimilant plus à un œdème localisé qu’à une compression mécanique et s’accompagnent d’un taux plus faible de bloc auriculoventriculaire (BAV)(3).
Au-delà de ces considérations anatomiques, la présence de troubles de conduction chez les patients candidats à un TAVI, plus importante que dans la chirurgie conventionnelle, s’explique aussi par l’âge élevé de ces patients.
Le bloc gauche (BBG) est le trouble conductif le plus fréquent en post-TAVI et son incidence est très variable selon le type de prothèse utilisé ; elle varie de 7 à 18 % pour les valves Edwards® et de 29 à 65 % pour les valves CoreValve®(4). Selon les séries, on observe un BAV dans 15,4 à 37,7 % des cas (tableau). Seulement 40 % des patients avec BBG évoluent vers un BAV. Dans plus de 90 % des cas, le BAV apparaît au cours de la procédure ou dans la semaine suivante, raison pour laquelle il est recommandé une surveillance étroite du rythme cardiaque pendant les 7 jours suivant la procédure.
Existe-t-il des facteurs prédictifs d’implantation de PM ?
Le taux d’implantation est supérieur avec la CoreValve®, en lien avec la position de sa « jupe ». On admet des taux d’implantation de 20 à 25 % avec la CoreValve®, et de 5 à 10 % avec les valves Edwards®(5). Le taux d’implantations peut par ailleurs varier d’un facteur 6 d’un centre à un autre, selon son activité.
Une métaanalyse publiée en 2010 et regroupant 2 047 patients, avait pour objectif de déterminer les facteurs prédictifs indépendants de BAV après TAVI nécessitant un appareillage(6).
Quatre facteurs principaux ont été retenus :
- l’utilisation d’une CoreValve® ;
- la présence préopératoire d’un BBD ;
- la survenue d’un BAV complet immédiat lors de la mise en place de la valve ;
- la profondeur d’implantation de la prothèse.
La présence d’un BBD préopératoire (4 à 14 % des patients) semble être le facteur prédictif le plus fort de survenue de troubles conductifs en post- TAVI avec un taux d’implantation de PM de 60 à 80 %.
La profondeur de la jupe sous l’anneau aortique détermine l’étendue de la zone de conduction touchée (figure 1)(7). Il existe peu de risque entre 4 et 8 mm. Une profondeur < 6 mm a donc été préconisée(8).
Figure 1. Impact du positionnement du stent valvé sur le système de conduction. En haut : Implantation haute dans la chambre de chasse. En bas : Implantation basse dans la chambre de chasse. (D’après C. Fracarro et al.(7)).
La taille de l’anneau aortique, lorsqu’elle est à la limite inférieure des valeurs pour lesquelles la valve est prévue, peut également favoriser un BAV(9).
Plus récemment, la durée du QRS en post-TAVI immédiat a été validée comme facteur fiable. En 2013, G. Mouillet et al., ont montré qu’en post-TAVI immédiat d’une CoreValve®, une durée du QRS supérieure à 128 ms est un facteur prédictif indépendant d’implantation de PM(10). Il est désormais admis que 120 ms serait un bon seuil pour gérer le patient sur le plan rythmique juste après l’intervention, et exclure les QRS fins de la perspective d’un PM (aucun patient présentant un QRS < 120 ms n’a eu de PM, et ceci avec un recul allant jusqu’à 50 mois).
Quelles sont les indications aujourd’hui ?
Des recommandations ont été établies pour l’implantation d’un PM en post- TAVI avec des indications absolues et d’autres plus relatives(11).
Le BAV de haut grade persistant : une indication absolue
Mais il n’y a pas de consensus sur le délai. Jusqu’à présent, une implantation précoce, dans les premiers jours postopératoires en cas de BAV de haut degré, était justifiée par le faible taux de récupération à court et moyen termes. Dans la plupart des études, l’implantation a lieu dans les 5 premiers jours, voire dans les 24 premières heures(6).
Ce délai rapide est remis en cause par plusieurs équipes qui préconisent une attitude plus attentiste. D’une part parce que l’implantation d’un PM, en particulier dans cette population, n’est pas dénuée de complications (3,4 % chez les patients de plus de 75 ans), d’autre part parce que le caractère transitoire de ces troubles conductifs a été démontré dans plusieurs séries. V. Guetta et son équipe ont observé une récupération de la conduction chez 60 % des patients implantés d’un PM en post-TAVI. Il en est de même pour L. Roten qui a constaté une récupération chez plus de 50 % des patients avec PM. Une autre étude a noté, après 1 an de suivi, que près de la moitié des patients bénéficiant de l’implantation d’un PM en postprocédure de TAVI ne sont pas dépendants(12-14).
Une attente plus prolongée, comme elle est par exemple préconisée dans les recommandations en postopératoire de chirurgie valvulaire, à 10 jours, permettrait d’éviter un certain nombre d’implantations (figure 2).
Comme dans le cas de la chirurgie, nous ne disposons pas d’études tranchantes pour déterminer une limite de temps certaine avant récupération de la conduction.
D’un autre côté, une attitude trop attentiste est à relativiser par les conséquences que peut entraîner une hospitalisation prolongée chez des sujets âgés, et cela d’autant que l’implantation d’un PM ne semble avoir aucun impact sur la mortalité à 1 an(1-15).
Figure 2. Évolution de la conduction chez un patient ayant fait l’objet d’un TAVI par prothèse CoreValve® (TAVI : implantation de prothèse aortique percutanée, BAV : bloc atrioventriculaire, PR : espace PR, BBG : bloc de branche gauche).
Les troubles conductifs –
BAV perprocédural transitoire, BAV de type 2, BBD associé à un PR long. Des indications relatives.
Le cas particulier du BBG.
La survenue d’un BBG concerne plus de la moitié des patients après TAVI. Le suivi à 1 mois, et dans certaines études à plus long terme, ne montre pas d’augmentation de recours à la stimulation définitive, ni de surmortalité cardiaque ou globale malgré la présence de ce BBG(8). Il ne constitue donc pas à ce jour une indication à la stimulation définitive.
En cas de BBG large, il faut néanmoins surveiller la tolérance hémodynamique et la fonction systolique ventriculaire gauche qui peuvent s’altérer par désynchronisation et aboutir à une indication de resynchronisation cardiaque. Il a été montré que les patients qui avaient les QRS les plus élargis après TAVI avaient le pronostic le plus péjoratif(16). La question sous-tendue par ces résultats est bien sûr la place de la stimulation multisite pour ces patients présentant un asynchronisme, que celui-ci soit le fait d’une stimulation VD permanente ou d’un bloc de branche gauche large après TAVI. Dans les cas de dysfonction systolique importante préexistante, le recours à la stimulation cardiaque triple chambre est communément admis en cas de BBG large (> 120 ms) après TAVI.
Conclusion
Le TAVI a connu ces 5 dernières années une expansion importante dans le monde compte tenu de ses excellents résultats cliniques.
Les troubles de la conduction peuvent être transitoires et le BBG peut ne pas relever d’une implantation. Il est primordial que les indications d’implantation de PM soient justement posées.
L’évaluation préalable est une étape importante afin de mettre à jour les facteurs prédictifs désormais reconnus d’implantation de stimulateur, dans le but d’anticiper la prise en charge des patients et d’orienter leur surveillance.
Attention, pour des raisons réglementaires ce site est réservé aux professionnels de santé.
pour voir la suite, inscrivez-vous gratuitement.
Si vous êtes déjà inscrit,
connectez vous :
Si vous n'êtes pas encore inscrit au site,
inscrivez-vous gratuitement :


