Trucs et astuces
Publié le 26 juin 2023Lecture 5 min
Réduire le risque d’hématome après implantation
Arnaud LAZARUS, Clinique Ambroise Paré, Neuilly-sur-Seine
C’est un sujet du quotidien et une des complications les plus fréquentes après implantation ou remplacement de dispositifs électroniques cardiaques implantables (DECI).
Fréquence
Selon les études, un hématome de loge (figure 1) survient dans 0,9 à 28,7 % des interventions de pose ou changement de DECI, avec un risque accru notamment par la présence d’un traitement antithrombotique.
Figure 1. Hématome postimplantation de DECI avec douleur et tension cutanée. Une reprise opératoire pour évacuation de l’hématome et complément d’hémostase sera nécessaire pour réduire le risque d’ouverture cutanée et lever la douleur.
Risques associés Douleur locale, nécrose ou ouverture cutanée (figure 2), réintervention pour évacuation et hémostase, infection, loge de DECI pathologique (adhérences, zone cutanée affinée), hospitalisation prolongée et surmortalité (2 % vs 0,7 %) sont des conséquences possibles. Une évacuation de l’hématome est ainsi nécessaire dans 0,3 à 2 % des cas et multiplie par 15 le risque d’infection.
Figure 2. Après un hématome significatif, il existe un risque accru d’avoir une loge pathologique avec parfois des adhérences et un affinement cutané localisé pouvant conduire à une extériorisation tardive de matériel.
Facteurs favorisants
Au premier plan on retrouve les troubles de l’hémostase, innés ou secondaires à une thrombopathie, à des traitements antiagrégants plaquettaires (plus encore en cas d’association double) et les anticoagulants oraux ou injectables qui majorent le risque de saignement et donc d’hématome. Jusqu’à 35 % des patients opérés pour un DECI suivent un traitement antiagrégant ou anticoagulant. Le type d’intervention compte aussi, les primo-implantations étant à plus faible risque. Pour diminuer le risque d’hématome, des actions peuvent être entreprises avant, pendant et après l’intervention.
Avant l’intervention
Contrairement à ce qui fut longtemps la règle, on ne fait plus de relais d’une anticoagulation orale par une héparinothérapie injectable. Cette attitude conduisait fréquemment à des phases de surdosage ou de sous-dosage de l’anticoagulation, avec les risques inhérents de saignement ou de thrombose.
Poursuivre les anticoagulants oraux (antivitamine K ou anticoagulants oraux directs) est dorénavant l’option la plus sûre au vu des résultats des études BRUISE CONTROL 1 (3,5 % d’hématomes sous warfarine vs 16 % en cas de relais héparinique) et BRUISE CONTROL 2 (taux inchangé d’hématomes de 2,1 %, que l’on maintienne ou interrompe les AOD avant l’intervention).
Alléger une double antiagrégation plaquettaire (si raisonnable au vu du risque de thrombose) ou interrompre brièvement un traitement anticoagulant non indispensable au moment de l’intervention peut aussi diminuer le risque de saignement (tableau), mais augmente en parallèle le risque d’AVC ischémique, d’infarctus ou d’embolie systémique. Cela peut cependant être envisagé par exemple chez un patient avec FA paroxystique mais en rythme sinusal stable depuis des mois, surtout si cela est conforté par les fonctions Holter d’un DECI (cas d’un changement de générateur).
D’après Glikson M et al. Eur Heart J 2021 ; 42(35) : 3427-520. AAP : antiagrégation plaquettaire ; AOD : anticoagulants oraux directs ; AVK : anti-vitamine K ; ACO : anticoagulants oraux ; PCI : intervention coronaire percutanée ; ClCr : clairance de la créatinine.
Pendant l’intervention
Il est préférable d’effectuer au début de l’intervention les gestes pouvant être source d’un saignement immédiat ou différé. C’est en particulier le cas de la loge d’implantation du DECI. Cela laisse le temps de s’assurer qu’aucun saignement notable ne se produit venant de la loge, cela alors que l’intervention se poursuit par ailleurs. L’hémostase doit bien sûr être la plus soigneuse possible, surtout chez les patients à risque accru de saignement (anticoagulants) ou d’infection. Pour réduire le risque de ponction artérielle sous-clavière ou axillaire, un abord vasculaire échoguidé peut être utilisé pour celles et ceux qui en ont l’expérience.
Il est parfois tentant de vouloir exciser des zones de tissu fibrotique au niveau de la loge, surtout lorsque la fibrose est abondante. Ce n’est pas forcément une bonne idée, car cette excision est fréquemment à l’origine de multiples zones de saignement, en nappes, ces suffusions hémorragiques étant difficiles à stopper.
Lors des changements de DECI, l’on est aussi parfois obligé d’agrandir la loge pour pouvoir y placer sans contraintes le nouveau DECI dont la forme ou le volume sont différents de l’ancien. Cet agrandissement concerne le plus souvent une partie de la loge éloignée de l’incision, donc avec une visibilité réduite pour identifier les sources de saignement et faire une bonne hémostase.
Les inserts hémostatiques n’ont pas vraiment emporté la conviction, bien qu’un effet favorable puisse parfois être obtenu. Ainsi, l’insertion dans la loge de 475 patients d’une éponge antibiotique lyophilisée imprégnée de collagène et de gentamycine a, rétrospectivement, significativement réduit le taux d’hématomes à 1 an (0,6 vs 13,8 % ; p < 0,001).
Après l’intervention
Il faut savoir prendre le temps d’effectuer une compression manuelle de plusieurs minutes si un saignement se produit lors de la suture cutanée, comme après le retrait d’une voie d’abord vasculaire.
Un pansement compressif n’est pas indispensable systématiquement, mais est préconisé en cas de traitement anticoagulant surtout si associé à une antiagrégation plaquettaire, pour couvrir le ou les premiers jours postopératoires. Toutefois, ces pansements posent parfois un problème de qualité de réalisation (niveau de compression et bon centrage de la compression) et de tolérance cutanée (allergie, érosion cutanée, inconfort des résidus de colle du pansement adhésif). La pose d’un poids en regard de la loge (sac de sable, voire de glace) est parfois utilisée mais avec un risque de glissement ou d’inconfort avec repositionnement ou retrait par le patient et donc d’inefficacité.
Partant de ce constat, certains ont développé des dispositifs de compression spécifiques tels que :
• PressRite, un système de compression pneumatique transparente réglable (figure 3). Sur 105 patients, 14,8 % d’hématomes sont survenus dans le groupe témoin contre 5,9 % avec PressRite, différence non significative mais sur un effectif faible.
Figure 3. Dispositif de compression pneumatique transparente.
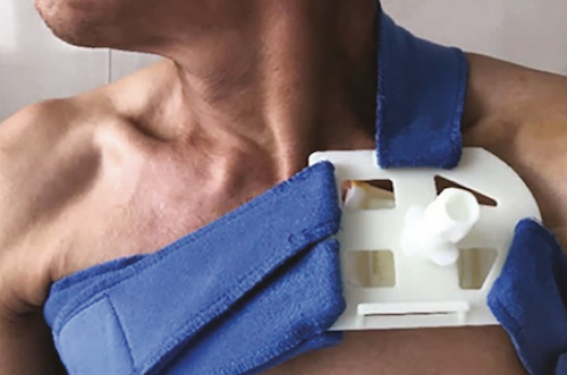
• Un autre dispositif permet une compression locale ajustable, ne nécessitant pas de pansement adhésif puisque le maintien est assuré par des sangles d’épaule et de thorax (figure 4). Testé sur 2 groupes de 102 patients sous AOD, comparativement à une compression mécanique par sac de sable, ce dispositif a permis de réduire le taux d’hématomes (11,8 % vs 36,3 % ; p < 0,01 – OR = 0,42 ; IC 95 % : 0,29-0,69 ; p = 0,01) et celui d’érosion cutanée (0 % vs 8,0 % ; p < 0,001), avec un meilleur confort.
Figure 4. Dispositif mécanique de compression avec sangles de maintien.
• Une veste de compression a également été imaginée, s’avérant efficace dans la prévention d’hématomes (0 % vs 30 % ; p = 0,002), notamment importants.
Attention, pour des raisons réglementaires ce site est réservé aux professionnels de santé.
pour voir la suite, inscrivez-vous gratuitement.
Si vous êtes déjà inscrit,
connectez vous :
Si vous n'êtes pas encore inscrit au site,
inscrivez-vous gratuitement :


