C Demain
Publié le 30 mar 2025Lecture 9 min
Prise en charge du syndrome du défilé neurologique par injection de toxine botulique
Pierre-Olivier THINEY, chirurgien vasculaire*, Alexandre SCHMITT, médecin physique et réadaptation, Martine LIEBGOTT, médecin vasculaire**, Gabriel FRANGER, médecin du sport* *Hôpital privé Jean Mermoz, Lyon **Centre Paul Santy, Lyon
Le syndrome du défilé thoracobrachial se présente sous trois formes : la forme artérielle, très rare (1 %), la forme veineuse peu fréquente (4 %) et la forme neurologique (N-TOS) qui représente la forme la plus courante (95 %). La prise en charge du N-TOS reste malgré tout controversée et n’est pas encadrée par des conférences de consensus. Néanmoins, il est d’usage de proposer en première intention dans le N-TOS de la kinésithérapie associée à la correction des troubles posturaux, ainsi que l’adaptation des pratiques sportives et/ou professionnelles. Afin d’améliorer la prise en charge conservatrice, certaines équipes ont proposé l’injection de corticostéroïdes ou d’anesthésiques locaux dans les muscles scalènes avec des résultats encourageants mais dont l’effet restait trop bref. Plus récemment, afin de prolonger l’effet, l’injection de la toxine botulique a été proposée.
Notre expérience
Méthodes
Après la confirmation du N-TOS, les patients étaient adressés en médecine physique et réadaptation pour une prise en charge ambulatoire. En fonction de l’examen clinique, 20 unités de toxine botulique (Xeomin®) étaient injectées dans les scalènes antérieurs, moyens et le petit pectoral sous guidage échographique. Le muscle sous-clavier n’a jamais été injecté.
En fonction des résultats de la première injection, une deuxième puis une troisième injection pouvaient être réalisées.
Les contre-indications habituelles sont : la myasthénie ou le syndrome de Lambert-Eaton, une injection de Botox® de moins de 3 mois, une grossesse en cours, l’allergie au Botox®, un traitement par aminosides et la bélénophobie (phobie des aiguilles).
Résultats
Soixante-seize patients porteurs d’un N-TOS ont été inclus de 2021 à 2023, majoritairement des femmes avec un âge moyen de 39 ans. L’ancienneté des symptômes était en moyenne de 85 mois (10-480 mois). Trente-deux patients présentaient une forme bilatérale, 24 sur le membre supérieur droit.
Dix-sept patients avaient un antécédent de traumatisme cervical, 47 une compression vasculaire asymptomatique et 27 étaient porteur d’une côte cervicale complète ou non, ou d’une apophysomégalie.
Les résultats ont été collectés de manière rétrospective sur un seul centre, avec un suivi moyen de 16 mois. Le critère d’évaluation principal était la comparaison du QuickDash test avant et après injection. Le QuickDash test a diminué de plus de 25 %, avec une différence statistiquement significative (p < 0,001).
Nous avons réparti les patients dans trois groupes d’évolution du QuickDash test* :
– entre 0 et 10 % d’amélioration : nous avons considéré que l’amélioration n’était pas significative. Ce groupe représente 30 % des patients traités ;
– entre 10 et 50 % d’amélioration : celle-ci a été considérée comme modérée. Ce groupe représente 38 % des patients traités ;
– plus de 50 % d’amélioration: elle a été considérée comme bonne. Ce groupe représente 32 % des patients traités.
*https://dash.iwh.on.ca/sites/dash/public/ translations/QuickDASH_French_Parisian.pdf.
Fayad F et al. Reliability, validity and responsiveness of the French version of the questionnaire Quick Disability of the Arm, Shoulder and Hand in shoulder disorders. Manual Therapy 2009 ; 14(2) : 206-12.
Au total, 70 % des patients ont eu une amélioration de modérée à bonne. Cinquante-cinq patients ont bénéficié d’une deuxième injection et 15 patients en ont reçu une troisième, avec un délai moyen de 4 mois entre chaque cycle d’injections. Les effets secondaires (23 %) ont été représentés uniquement par des effets mineurs comme des douleurs locales, de la toux et une asthénie. Vingt-huit patients ont pu reprendre une activité professionnelle normale, cinq restent en temps partiel, 14 patients ont dû se reconvertir professionnellement et 27 demeurent malgré tout en arrêt de travail.
Malgré les injections de toxine botulique, 26 patients ont dû bénéficier d’une neurolyse du plexus brachial avec résection des scalènes, de la première côte et souvent une ténotomie du petit pectoral par voie sus- et sous-claviculaire.
Cette prise en charge a été retenue dans deux indications :
– l’absence d’effet du Botox® ;
– l'efficacité du Botox® mais de durée d’action trop courte.
Nous avons analysé le sexe, la présence d’une côte cervicale, l’ancienneté des symptômes, un antécédent de traumatisme cervical, la présence d’une compression vasculaire asymptomatique, le nombre de muscles injectés, et aucun de ces critères n’a influencé les résultats dans notre expérience.
Discussion
Limites de la rééducation par kinésithérapie
La prise en charge par kinésithérapie du N-TOS reste un challenge à plusieurs niveaux. En effet, la prescription de rééducation initiée souvent par les chirurgiens vasculaires se résume en général à une prescription « type » unique qui n’est souvent pas adaptée au morphotype du patient. La rééducation est différente entre une patiente de profil « hypotonique » de type « Droopy syndrom » et un patient amateur de crossfit avec une hypertrophie des scalènes.
Par ailleurs, l’évaluation de la rééducation s’appuie sur une littérature hétérogène aux sources souvent anciennes. On rappelle que le protocole de PEET de la Mayo Clinic date de 1956 s’appuyant sur une série monocentrique rétrospective de 55 patients. Ces éléments expliquent que la rééducation seule offre des résultats incertains et parfois décevants.
Modes d’action de le toxine botulique
• Action myorelaxante
La toxine botulique est une neurotoxine produite par Clostridium botulinum, responsable du botulisme lorsqu’elle est ingérée. Elle est utilisée en thérapeutique principalement pour ses propriétés myorelaxantes. Une fois injectée dans le muscle, la toxine botulique va inactiver le complexe SNARE qui intervient dans le « docking » vésiculaire, bloquant ainsi l’exocytose de l’acétylcholine au niveau du nerf moteur. La conséquence directe est un blocage de la plaque motrice, responsable d’une chémodénervation irréversible.
• Action antalgique
La toxine botulique possède également une action antalgique propre en limitant la production de médiateurs pro-inflammatoires et en bloquant les neurones nocicepteurs.
Évaluation de l’utilisation du Botox® dans la littérature
Les études actuelles évaluant la toxine botulique dans la prise en charge du N-TOS sont peu nombreuses. Seul un seul essai randomisé a comparé la toxine botulique au sérum physiologique sans démontrer de réelle efficacité**. Les auteurs justifiaient cette absence d’amélioration par des biais entre le groupe placebo et le groupe toxine botulique, notamment sur l’ancienneté des symptômes. Néanmoins, les études bien qu’hétérogènes souvent rétrospectives et monocentriques semblent montrer un effet positif de la toxine botulique dans la prise en charge N-TOS.
** Finlayson HC, et al. Botulinum toxin injection for management of thoracic outlet syndrome: A double-blind, randomized, controlled trial. Pain 2011 ; 152(9) : 202.
L’absence de critères diagnostiques uniformes pour le N-TOS complique par ailleurs la comparaison des résultats entre les études. Plusieurs articles suggèrent que la bonne réponse à la toxine botulique est un bon indicateur de succès pour une éventuelle chirurgie de neurolyse du plexus brachial. S’il n’y a pas de consensus sur le nombre de muscles à injecter, il semble cependant que d’injecter les scalènes antérieur, moyen et le petit pectoral offre de meilleurs résultats que l’injection ciblée d’un seul muscle.
Les principaux effets secondaires décrient sont des douleurs musculaires, un syndrome grippal, la toux et, rarement, une faiblesse perceptible du muscle injecté. Ils sont rares et mineurs.
• Quel dosage ?
Dans notre expérience, en général 20 unités de toxine botulique ont été injectées dans chaque muscle. La revue de la littérature montre que les données sont également hétérogènes, puisque certains auteurs administrent entre 10 et 75 unités par muscle. Cette absence de consensus explique également l’hétérogénéité des résultats.
• Quel guidage ?
Plusieurs types de guidage sont décrits pour effectuer l’injection : l’échographie, l’EMG, la fluoroscopie et le scanner. Si aucune méthode de guidage ne semble supérieure dans la revue de la littérature, l’échographie semble offrir l’avantage d’être plus accessible, de réduire les coûts et l’exposition aux radiations.
• Quelle est la durée d’action du Botox® ?
L’efficacité de l’injection est limitée dans le temps. En effet, il existe des phénomènes de réinnervation musculaire qui surviennent en 3 à 4 mois (sprouting). Ceci explique l’effet parfois transitoire de l’injection de Botox®. Or dans notre expérience, certains patients n’ont bénéficié que d’un ou deux cycles d'injections avec un effet définitif. Nous expliquons cela par le fait que l’injection de toxine botulique dans les muscles permet de réduire leur contracture chronique, interrompant ainsi le cycle de la douleur. Cette diminution des tensions musculaires facilite ainsi une rééducation efficace.
Les toxines botuliques sont-elles indiquées dans les formes vasculaires ?
L’utilisation de le toxine botulique dans les formes vasculaires n’a été décrite que dans un seul case report en 2008. Néanmoins, l’utilisation de la toxine botulique dans les formes vasculaires de syndrome du défilé ne semble pas justifiée pour plusieurs raisons :
– dans la forme veineuse, la compression est souvent dans la pince costoclaviculaire au contact du muscle subclavier qui n’est pas accessible aux injections de toxine botulique ;
– concernant la forme artérielle, les bons résultats de la chirurgie et la nécessité d’avoir un résultat définitif sur l’artère justifient de ne pas proposer la toxine botulique dans cette indication.
Le Botox® est-il indiqué dans les formes neurologiques avec une côte cervicale ?
Ce cas de figure n’est pas clairement évalué dans la littérature. De notre expérience, les formes de N-TOS avec côte cervicale étant les seules à engendrer des complications neurologiques de type troubles de conduction à l’EMG ou amyotrophie, il paraît nécessaire de proposer au patient un traitement définitif que n’offre pas toujours le Botox®. Par ailleurs, les douleurs ressenties par le patient dans ce cas sont en rapport à un conflit neuro-osseux entre les racines du plexus brachial et la côte cervicale. L’action myorelaxante du Botox® ne semble donc pas utile dans cette indication.
Conclusion
Bien que les résultats de la littérature et notre expérience manquent de puissance et soient hétérogènes, il semble néanmoins que la toxine botulique a dans certains cas un effet favorable sur le N-TOS. Les effets secondaires étant rares et mineurs, il semble légitime d’intégrer la toxine botulique dans l’arsenal thérapeutique de la prise en charge du N-TOS. La réponse au Botox® semble par ailleurs être un critère prédictif de succès de la chirurgie de neurolyse du plexus brachial.
Malgré tout, l’utilisation de la toxine botulique dans cette indication devrait être réévaluée dans le cadre de cohortes prospectives de plus grande envergure, avec des résultats standardisés afin de mieux définir sa place dans cette indication.
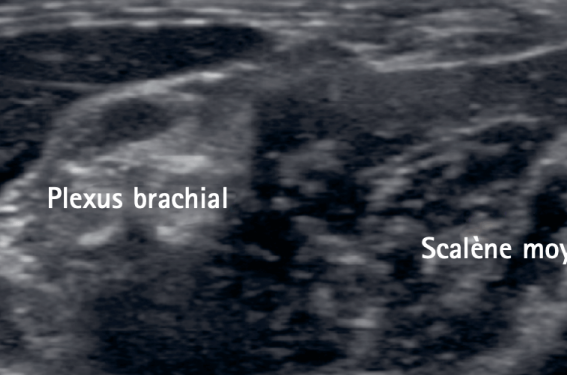
Figure 1. Coupes échographiques « out plane » illustrant l’injection du scalène antérieur et moyen (images du Dr Alexandre Schmitt).
Figure 2. Coupe échographique « in plane » montrant l’injection du petit pectoral (images du Dr Alexandre Schmitt).
Figure 3. Stratégie de prise en charge des N-TOS traités par Botox®.
Pour en savoir plus :
• Peet RM, Henriksen JD, Anderson TP, Martin GM. Thoracicoutlet syndrome: Evaluation of a therapeutic exercise program. Proc Staff Meet Mayo Clin 1956 ; 31(9) : 281-7.
• Arnon SS, Schechter R, Inglesby TV et al. ; Working Group on Civilian Biodefense. Botulinum toxin as a biological weapon: Medical and public health management. JAMA 2001 ; 285(8) : 1059-70.
• Woodworth TT, Le A, Miller C, et al. Botulinum toxin injections for the treatment of neurogenic thoracic outlet syndrome: A systematic review. Muscle Nerve 2024 ; 70(1) : 28-35.
• Finlayson HC, O’Connor RJ, Brasher PMA et al. Botulinum toxin injection for management of thoracic outlet syndrome: A double-blind, randomized, controlled trial. Pain 2011 ; 152(9) : 2023-8.
• Danielson K, Odderson IR. Botulinum toxin type A improves blood flow in vascular thoracic outlet syndrome. Am J Phys Med Rehabil 2008 ; 87(11), 956-9.
Attention, pour des raisons réglementaires ce site est réservé aux professionnels de santé.
pour voir la suite, inscrivez-vous gratuitement.
Si vous êtes déjà inscrit,
connectez vous :
Si vous n'êtes pas encore inscrit au site,
inscrivez-vous gratuitement :


