Insuffisance cardiaque
Publié le 14 avr 2016Lecture 8 min
Insuffisance cardiaque aiguë et syndrome cardiorénal
H. PRIGENT, D. LOGEART, CHU Lariboisière, Paris
L’existence ou l’apparition d’une insuffisance rénale (IR) est un marqueur pronostique fort dans l’insuffisance cardiaque (IC), aiguë (ICA) ou chronique (ICC) : les patients qui développent une insuffisance rénale ont une mortalité jusqu’à 2 fois plus élevée que les patients sans insuffisance rénale(1). En effet, la fonction rénale, sa dégradation ou son amélioration sont des marqueurs de l’équilibre et de la gravité de l’IC. Le cœur et la stimulation neuro-hormonale sont dépendants de la régulation de la balance hydrosodée par le rein et vice versa. Toute altération du fonctionnement de l’un entraîne un dysfonctionnement de l’autre, et est désigné sous le terme de syndrome cardiorénal (SCR). Il y a quelques années, Ronco et coll. avaient défini plusieurs types de syndrome cardiorénal selon que le cœur ou le rein sont l’acteur ou la cible(2). Nous abordons ici l’altération de la fonction rénale secondaire à l’IC dans le contexte d’IC aiguë ou décompensée, et ses conséquences thérapeutiques.
À défaut d’être consensuelle, la définition de la dégradation de la fonction rénale est basée depuis de nombreuses années sur un seuil d’augmentation de créatininémie de 0,3 mg/l ou 26,5 micromoles/l. En cas d’IC aiguë, une telle dégradation de la fonction rénale survient chez 25 % des patients.
Le rein du patient insuffisant cardiaque est exposé à plusieurs facteurs qui vont altérer son fonctionnement(2,3) :
Une baisse chronique du débit de perfusion : ce phénomène a été récemment relativisé dans l’ICC car le rein dispose de mécanismes d’autorégulation, via notamment les phénomènes de vasoconstriction des artérioles pré- ou post-rénales. Cependant, en cas de baisse brutale du débit cardiaque, ce mécanisme devient central.
Une congestion chronique ou des épisodes de congestion veineuse répétés. La congestion entraîne une diminution de la pression de perfusion rénale, une inflammation chronique, source d’IRA puis, si le phénomène persiste, d’IRC. Les études des dernières années insistent sur la prééminence hémodynamique de ce phénomène(4).
Une activation neuro-hormonale chronique, avec une activation du SRAA et du système arginine vasopressine, générant une véritable néphropathie vasomotrice avec vasoconstriction intrarénale prononcée.
Ces mécanismes se surajoutent éventuellement à une maladie rénale prémorbide chez les patients diabétiques, hypertendus, mais aussi à la iatrogénie (produits de contraste iodés, anti-inflammatoires, antibiotiques, diurétiques pourvoyeurs d’hypovolémie parfois délétère) et à d’autres facteurs aggravants tels que l’anémie, l’hyperurémie, etc.
Le rein de l’insuffisant cardiaque chronique a la particularité d’avoir une fenêtre de volémie optimale extrêmement étroite (figure 1), très sensible à la congestion, mais aussi à l’hypovolémie.
Figure 1. La fenêtre thérapeutique est étroite dans le maniement de la volémie du patient insuffisant cardiaque avec un rein fragilisé (Ronco et al. Eur Heart J 2013).
Ainsi, tout l’art de la prise en charge est d’évaluer au mieux la volémie en aigu et au long cours, pour optimiser le traitement, permettant d’équilibrer de manière durable l’ICC tout en minimisant les agressions rénales répétées, parfois pourtant inéluctables.
Évaluation de la volémie et de la fonction rénale
L’évaluation de la volémie est à la fois un paramètre essentiel et une vraie difficulté clinique dans bien des cas. La volémie est le volume sanguin total mais en cas de congestion, il y a aussi une inflation hydrosodée du secteur interstitiel (« 3e secteur ») avec des mouvements de transfert vers ou depuis le secteur vasculaire qu’il faut prendre en compte. Les réanimateurs définissent la volémie optimale via le concept de « précharge-dépendance » du débit cardiaque. Dans l’IC gauche ou globale traitée par le cardiologue, le niveau de remplissage vasculaire idéal est bien difficile à définir et correspond finalement à celui qui permettra l’équilibre le plus durable, à savoir des hospitalisations les plus espacées possibles. Les signes cliniques sont assez souvent pris en défaut : l’hypervolémie, mesurée par exemple par marquage radioactif, peut exister en l’absence de tout signe clinique de congestion(5). L’impédancemétrie thoracique a des résultats mitigés et est peu répandue en milieu cardiologique. L’échographie permet une estimation des pressions de remplissage gauche et droite et une mesure de la compliance et de la taille de la veine cave mais ces paramètres sont aussi parfois pris en défaut. La détection de lignes B de Kerley pulmonaires peut se faire en échographie et signent une surcharge interstitielle pulmonaire ; sa valeur ajoutée mérite d’être mieux évaluée. Les taux de BNP ou NT-proBNP sont corrélés davantage aux contraintes ventriculaires qu’à la seule volémie et la cinétique rapprochée des taux est mal corrélée à la volémie.
Concernant la fonction rénale, la créatinine est un paramètre tardif de dégradation et imprécis en cas de DFG préalablement abaissé. L’augmentation de créatininémie ne survient que 24 à 48 h après les dégâts rénaux, fonctionnels ou organiques.
De nouveaux biomarqueurs pourraient permettre une évaluation plus fine. Plusieurs paramètres biochimiques simples aident à identifier l’IR dite « fonctionnelle » ou « prérénale », c’est-à-dire liée à l’hémodynamique et en partie réversible : chute de la natriurèse < 20 mmol/l, rapport Na/K urinaire < 1, augmentation du rapport urée/créatinine (ou créatinine U/P > 40 ; urée U/P > 100), fraction excrétée de l’urée < 35 % (urée urinaire x créatinine plasmatique)/( urée plasmatique x créatinine urinaire). La cystatine C est une protéine synthétisée à un taux relativement constant par toutes les cellules nucléées, filtrée librement et complètement réabsorbée par le tubule proximal, sans être sécrétée dans l’urine. Son taux sanguin n’est affecté ni par l’âge, ni par le genre, la race ou la masse musculaire. Elle est un meilleur prédicteur de la fonction glomérulaire que la créatinine. Enfin, des biomarqueurs précoces d’ischémie tubulaire ont été identifiés — NGAL, KIM-1 — mais leur intérêt clinique dans le contexte de suivi d’une insuffisance cardiaque n’es t pas démontré(6).
Prise en charge thérapeutique
Que retenir une fois que l’on sait que les outils utilisés en pratique courante sont, isolément, insuffisants pour prédire la volémie et évaluer la fonction rénale à l’instant t ?
La première règle est d’avoir une approche multiparamétrique.
Le clinicien doit tenir compte de l’histoire clinique de chaque patient et intégrer les différents paramètres clinico-biologiques. La deuxième est que le patient présentant ou développant une insuffisance rénale ne doit pas faire l’objet d’un traitement minimaliste par crainte de l’insuffisance rénale car ce sont l’obtention d’une « euvolémie » et la titration du traitement par inhibiteur du SRAA, bêtabloquants et antialdostérone qui sont les meilleurs garants de la stabilité du patient.
Quelques points importants
• Décongestionner
Les patients en IC globale décompensée ont besoin d’un traitement diurétique intensif. L’étude CARESS-HF (traitement randomisé ultrafiltration versus traitement diurétique agressif) a introduit un schéma thérapeutique personnalisé, évalué quotidiennement sur la diurèse, avec des doses importantes de diurétiques de l’anse par voie IV (120 mg/j au minimum) avec une escalade rapide pour un objectif de diurèse entre 3 et 5 litres)(7).
• Associer les diurétiques
Utiliser un diurétique thiazidique introduit dès J2-J3 et un inhibiteur du SRAA pour éviter la stimulation du SRAA par les diurétiques de l’anse eux-mêmes, et empêcher la réabsorption compétitive de sodium à d’autres endroits dans les tubules rénaux.
• Respecter l’hémoconcentration
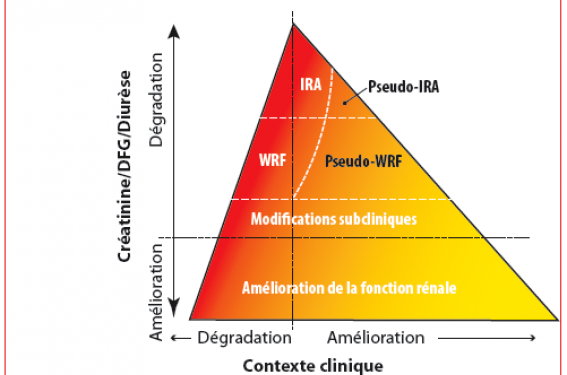
Une fois le patient bien déplété, il arrive souvent que la créatinine remonte, après avoir initialement baissé. Il s’agit alors d’adapter les doses de diurétiques sans les arrêter complètement et de revoir le patient de manière rapprochée. Le pronostic du patient IC qui dégrade sa fonction rénale de façon concomitante à une évolution clinique favorable, n’est pas altéré (figures 2 et 3).
On peut ainsi tolérer une dégradation de la fonction rénale modérée si elle reflète une hémoconcentration ; la fonction rénale s’équilibre ensuite.
Figure 2. Survie en fonction de la volémie chez l'insuffisant cardiaque : les patients hémoconcentrés ont une meilleure survie. (Testani JM et al. Circulation 2010).
Figure 3. Toute dégradation de la fonction rénale n'a pas le même pronostic, il faut corréler la dégradation rénale à l'évolution clinique. Une dégradation de la fonction rénale concomitante d'une amélioration clinique n'a pas de signification péjorative, contrairement à l’IR du patient qui ne répond pas au traitement médical de l’IC. (Damman et al. Eur Heart J 2015). IRA = insuffisance rénale aiguë. WRF = aggravation de la fonction rénale.
• Savoir identifier et prendre en charge la résistance aux diurétiques
À ne pas confondre avec des doses de diurétiques insuffisantes. En cas de résistance aux diurétiques avérée, seules l’hypo - perfusion rénale majeure ou la congestion rénale peuvent être réversées au moins transitoirement. Peuvent être discutés les inotropes et/ou l’ultrafiltration mais aussi à plus ou moins court terme l’assistance et/ou la greffe cardiaque.
• Savoir proposer l’ultrafiltration chez certains patients « réfractaires »
L’ultrafiltration (UF) permet de diminuer directement la congestion veineuse sans recours aux inotropes. Elle présente l’avantage, au moins théorique, de retirer un liquide iso-osmolaire (la diurèse induite par les diurétiques est hypo-osmolaire), permettant une plus grande perte nette de fluide, une moindre activation neuro-hormonale et de générer moins de déséquilibres ioniques (hypokaliémie). Son efficacité clinique a été évaluée dans plusieurs essais randomisés sur des effectifs restants modestes. Les résultats sont mitigés à ce jour : bénéfiques dans UNLOAD (UF versus traitement médical agressif)(8) ; négatifs dans CARESS-HF (UF versus traitement médical agressif. L’autre alternative est bien souvent la dobutamine mais son inocuité est contestable à moyen terme.
• Introduire les IEC et antialdostérone à un moment opportun
Les IEC ont un bénéfice important chez les patients IC, y compris avec une insuffisance rénale (figure 4). Les IEC et ARA2 modifient l’hémodynamique intrarénale et réduisent la fraction de filtration glomérulaire. C’est un mécanisme protecteur en cas d’hypertension artérielle, de néphropathie diabétique, de maladie inflammatoire glomérulaire et de toute néphropathie avec albuminurie. Mais cet effet protecteur perd tout son sens en cas de congestion rénale aiguë par exemple ou à l’inverse d’aggravation rénale du fait d’une hypovolémie iatrogène sévère. Ainsi, il faut savoir introduire des IEC, mais aussi les arrêter ou les diminuer en cas d’IRA. Les antialdostérones ne modifient pas l’hémodynamique intrarénale mais exposent au risque d’hyperkaliémie, nécessitant une surveillance étroite de la kaliémie chez ces patients.
• Rechercher la carence martiale et la corriger, même en l’absence d’anémie(9).
• Surveiller très régulièrement l’ionogramme sanguin chez tout IC sous diurétiques et bloqueur du SRAA, notamment en cas de sévérité ou d’instabilité.
• Adresser le patient au néphrologue avant que l’insuffisance rénale n’atteigne le stade terminal, c’est-à-dire dès que le DFG est inférieur à 45 ml/min/m2. Certains patients peuvent par exemple bénéficier d’une dialyse péritonéale avant le stade d’IR terminale pour équilibrer la volémie(10,11). Il est nécessaire d’établir un partenariat avec une équipe de néphrologues.
Figure 4. L’introduction du valsartan chez un patient avec un DFG altéré s’accompagne d’une dégradation rénale plus importante que sous placebo. Pourtant, malgré cette dégradation initiale, le bénéfice sur les événements cardiovasculaires se maintient chez ces patients par rapport au placebo et est même plus marqué que chez les patients sans altération du DFG. (Lesogor et al. Eur J Heart Fail 2013).
Attention, pour des raisons réglementaires ce site est réservé aux professionnels de santé.
pour voir la suite, inscrivez-vous gratuitement.
Si vous êtes déjà inscrit,
connectez vous :
Si vous n'êtes pas encore inscrit au site,
inscrivez-vous gratuitement :