Rythmologie et rythmo interventionnelle
Publié le 31 mai 2016Lecture 4 min
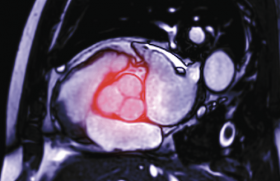
Morphologie et fonction de l’oreillette gauche dans la fibrillation atriale
F. SCHNELL, Laboratoire de physiologie, Université Rennes 1 ; Service de cardiologie, service de médecine du sport, CHU Pontchaillou, Rennes, Inserm UMR 1099

Le remodelage morphologique progressif de l’oreillette gauche dans de nombreuses pathologies cardiovasculaires va être à l’origine d’un remodelage électrique qui fait le lit de la fibrillation atriale (FA). La FA elle-même va induire un remodelage structurel et fonctionnel.
Prévalence de la FA
La prévalence de la fibrillation atriale (FA) dans les pays développés est de 1,5 à 2 % de la population générale, avec un âge moyen de 75 à 85 ans. Cette arythmie est associée à une augmentation du risque d’AVC, d’insuffisance cardiaque et de mortalité. Le dépistage précoce de cette pathologie fréquemment silencieuse est indispensable, permettant une introduction rapide des thérapeutiques appropriées, notamment les anticoagulants, et permettant dans certains cas de mettre en place de stratégies de prévention de progression de la maladie(1).
Remodelage de l’oreillette gauche dans la FA
La majorité des pathologies cardiovasculaires (HTA, infarctus, valvulopathies, etc.) sont à l’origine d’un remodelage morphologique progressif des oreillettes. Dans les oreillettes, va se produire une différenciation de fibroblastes en myofibroblastes et un dépôt de tissu conjonctif et de fibrose. On assiste ainsi à une altération de la fonction atriale et à une dilatation de l’oreillette gauche (OG). Ce remodelage morphologique va être à l’origine d’un remodelage électrique avec la création de circuits de réentrées qui vont favoriser l’apparition de la FA. Une fois installée, la FA en ellemême va induire un remodelage structurel et fonctionnel qui va entraîner une progression de la pathologie. Ainsi, la FA paroxystique devient permanente et la chance de succès d’une cardioversion diminue au fil du temps. Sur le plan électrophysiologique, les changements au niveau des mécanismes cellulaires et de canaux ioniques vont conduire à une diminution de la période réfractaire atriale(2). Sur le plan hémodynamique, la FA est responsable d’une perte de la contraction synchronisée des oreillettes, ce qui diminue le débit cardiaque de 5 à 15 %. Cet effet est bien sûr plus marqué lorsque la compliance VG est réduite, puisque que la contribution de la contraction atriale dans le remplissage du VG est plus importante. Le risque d’accident vasculaire cérébral (AVC) et d’embolie systémique chez les patients en FA est lié à de nombreux mécanismes physiopathologiques, notamment la stase sanguine dans l’auricule gauche, qui est la principale source d’embolie.
Impact pronostique et thérapeutique de l’évaluation du remodelage atrial gauche dans la FA
Même si les recommandations actuelles ne prennent pas en compte le remodelage morphologique atrial dans la stratégie thérapeutique concernant le traitement antiarythmique et anticoagulant, de nombreuses études s’intéressent à l’apport de l’imagerie pour mieux stratifier le risque de récidive après cardioversion ou le risque d’embolie.
Dilatation OG
Des études prospectives ont démontré qu’une dilatation de l’OG était associée au risque de développer de la FA(3), à sa transformation en FA permanente(4), ainsi qu’à un risque accru de récidive après cardioversion ou ablation endocavitaire(5). La taille de l’OG est également associée au risque embolique. La valeur supérieure de la normale du volume OG dans la population générale est de 41 ml/m2(6,7).
Fonction OG
Il est possible de mettre en évidence une altération de la fonction atriale, même après le retour en rythme sinusal et en l’absence de dilatation OG. En effet, même après une cardioversion, il existe fréquemment une perte de la contraction atriale.
Cette dysfonction de contraction atriale est corrélée à la durée de la FA et il faut parfois plusieurs mois avant que la fonction atriale récupère totalement(8). Ceci explique qu’il est nécessaire de conserver un traitement anticoagulant jusqu’à 4 semaines après une cardioversion(1).
En effet, des études ETO ont démontré qu’il était possible d’avoir une formation de thrombi atriaux de manière précoce après une cardioversion.
Différents outils peuvent être utilisés pour quantifier la fonction atriale gauche. En échocardiographie, on peut utiliser une approche volumétrique, l’imagerie de déformation myocardique, ou l’évaluation de la fonction de l’auricule gauche par la vitesse des flux en ETO.
La vitesse de vidange de l’auricule gauche, mesurée au cours d’une échocardiographie transœsophagienne, est un indice de contractilité auriculaire. Cet indice est prédictif du risque de thrombus intra-atrial, mais également prédictif d’un succès de cardioversion, avec une valeur seuil de 40 cm/s(9).
Par rapport aux données volumétriques, la technique du 2D strain présente l’avantage de pouvoir quantifier les différentes fonctions atriales de l’OG avec une bonne reproductibilité (variabilité intraobservateur : 8 % et interobservateur 9,5 %)(10). Cette technique permet de quantifier les 3 rôles physiologiques majeurs de l’OG, c’est-à-dire la fonction de pompe contractile, la fonction de réservoir durant la systole ventriculaire et la fonction de conduit durant la diastole ventriculaire (figure).
En FA, la fonction pompe contractile est perdue, la fonction réservoir et la fonction conduit sont réduites, avec une altération plus marquée en cas de FA persistante qu’en cas de FA paroxystique. Le degré d’altération de la fonction réservoir est corrélée au score de CHA2DS2-VASc et est prédictif d’AVC et de mortalité chez les patients en FA. Elle est également prédictive du maintien en rythme sinusal(11).
Figure. Physiologie de l’oreillette.
En pratique
Même si les recommandations actuelles ne prennent pas en compte le remodelage morphologique atrial dans la stratégie thérapeutique, il est probable que dans le futur, l’étude de la fonction de l’oreillette gauche permettra d’avancer dans l’optimisation de la sélection des patients candidats à l’ablation endocavitaire.
Cela pourra également influencer la décision de débuter un traitement anticoagulant.
Attention, pour des raisons réglementaires ce site est réservé aux professionnels de santé.
pour voir la suite, inscrivez-vous gratuitement.
Si vous êtes déjà inscrit,
connectez vous :
Si vous n'êtes pas encore inscrit au site,
inscrivez-vous gratuitement :