Publié le 14 juin 2005Lecture 9 min
Insuffisance cardiaque aiguë
J.-L. DUBOIS-RANDÉ, E. VERMES et M. KIRSCH, hôpital Henri Mondor, Créteil
Les progrès réalisés dans les systèmes d’assistance circulatoire ont modifié la prise en charge de l’insuffisance cardiaque aiguë.
La prise en charge médicamenteuse n’a pas vraiment changé mais les modes de ventilation optimaux sont désormais bien connus des réanimateurs.
L'insuffisance cardiaque aiguë est souvent le mode de décès des patients souffrant d’une insuffisance cardiaque chronique. Ces patients ont été traités durant des années par des médicaments qui ont permis de reculer cette phase terminale. Ils sont le plus souvent âgés et hors des délais raisonnables de la transplantation (tableau 1). Cela rend en général difficile la mise en place d’une assistance circulatoire, dont les chances de succès sont d’autant plus grandes que la personne est jeune.
Le choc cardiogénique de l’infarctus du myocarde garde une incidence et une mortalité fortes. La revascularisation myocardique par angioplastie a peu diminué la mortalité des patients en état de choc, surtout du fait de leur arrivée tardive à l’hôpital. La décision d’assistance doit donc être prise en urgence avant une dégradation polyviscérale ou la survenue d’un trouble du rythme.
Épidémiologie de l’insuffisance cardiaque aiguë
Il existe peu de données épidémiologiques sur l’insuffisance cardiaque aiguë qui survient le plus souvent sur une cardiopathie évoluée connue ou méconnue. On distingue les insuffisances cardiaques droites des insuffisances cardiaques gauches. Il s’agit d’une distinction assez artificielle en raison de l’interdépendance des ventricules : une insuffisance cardiaque gauche retentit sur le cœur droit.
Dans un registre français récent, EFICA (Étude d’observation Française d’Insuffisance Cardiaque Aiguë), mené dans des centres de cardiologie représentatifs : l’âge moyen était de 70 ans avec une majorité d’hommes (60 %). L’étiologie dominante était une cardiopathie ischémique. Dans près de 40 % des cas, le facteur déclenchant était de cause ischémique, suivi en fréquence par les troubles du rythme. La mortalité était de l’ordre de 30 %. Dans le cas de l’infarctus du myocarde, entre 7 et 10 % des patients se présentent en état de choc cardiogénique dont la fréquence a peu varié dans la dernière décennie.
Aspects physiopathologiques
L’insuffisance cardiaque aiguë se définit comme l’incapacité brutale de la pompe cardiaque à assurer, dans des conditions de retour veineux adéquat, les besoins métaboliques de l’organisme, en particulier en oxygène. On distingue habituellement trois grands types d’insuffisance cardiaque aiguë :
• l’insuffisance circulatoire où prédomine l’atteinte périphérique,
• l’insuffisance cardiaque secondaire à une atteinte essentiellement mécanique (valve ou péricarde),
• l’insuffisance cardiaque secondaire à une atteinte directe du myocarde.
D’un point de vue clinique, en fonction du degré de congestion, on distingue les insuffisances cardiaques non ou peu congestives et les insuffisances cardiaques congestives. Cette distinction clinique est de fait très subjective et théorique dans la mesure où des signes d’hypoperfusion périphérique peuvent être associés à des signes de congestion comme dans le cas du choc cardiogénique.
Au stade d’insuffisance cardiaque, plusieurs anomalies de la courbe pression-volume sont observées.
Dans l’insuffisance systolique, la pente de la relation pression-volume télésystolique est abaissée, traduisant l’altération contractile.
Dans l’insuffisance cardiaque dite diastolique le volume d’éjection et le débit cardiaque sont maintenus mais au prix d’une augmentation très importante des pressions de remplissage.
En clinique, les deux entités coexistent surtout dans les cardiopathies sévères (figure 1). La recherche d’un facteur déclenchant est une règle.
Figure 1. Relation pression-volume. Cœur normal et cœur pathologique.
Méthodes d’évaluation
L’échocardiographie est aujourd’hui déterminante dans l’abord d’une insuffisance cardiaque aiguë. Elle va non seulement contribuer au bilan étiologique mais elle permet également actuellement une évaluation hémodynamique assez complète, dont le bilan des désynchronisations (intra- et interventriculaires), très déterminante pour poser l’indication d’une stimulation triple chambre qui est un traitement reconnu de certaines insuffisances cardiaques graves.
L’hémodynamique invasive a une place moindre aujourd’hui mais est la seule technique permettant de mesurer les résistances pulmonaires. Elle est éventuellement associée à des épreuves pharmacologiques.
Approches thérapeutiques en dehors de l’assistance circulatoire
Il n’y a pas eu de grandes modifications dans l’approche thérapeutique. Les inotropes restent en première ligne. Parmi ces derniers, la dobutamine a une place prépondérante, associée ou non à la dobutamine. L’adrénaline garde aussi une large place, surtout face à des résistances systémiques basses. Le maintien des bêtabloquants chez un patient qui en prenait de façon chronique pourrait peut-être modifier le pronostic, même dans ces formes graves. Récemment, le BNP intraveineux a montré des résultats intéressants ainsi que de nouveaux inotropes.
Dans le cas du choc cardiogénique de l’infarctus du myocarde, l’angioplastie en urgence apporte un bénéfice en termes de morbi-mortalité. La contre-pulsion aortique facilite le geste d’angioplastie mais n’a pas apporté de bénéfice net sur la mortalité.
Assistance circulatoire
La raréfaction du nombre de donneurs, qui s’aggrave depuis 1993, constitue un des facteurs limitant la transplantation cardiaque. Parallèlement, environ 15 % des patients inscrits sur liste de transplantation cardiaque décèdent. C’est dans ce contexte que le développement des techniques d’assistance circulatoire a été favorisé (figure 2). De nombreux dispositifs d’assistance mécanique existent, plus ou moins complexes, permettant un traitement efficace dans l’attente de la récupération d’un cœur natif ou de la transplantation cardiaque.
Les principales indications sont le choc cardiogénique secondaire à un infarctus ou un processus inflammatoire, et les décompensations aiguës d’une cardiomyopathie chronique. Dans les deux premiers cas, une éventuelle récupération myocardique peut être envisagée, la dernière indication est en attente de transplantation.
Le choix d’un système doit se faire selon plusieurs critères : degré d’urgence, attente de récupération ou attente de transplantation, durée probable de l’assistance, ventricule à assister (gauche ou droit et gauche), débit d’assistance souhaité. Nous développerons principalement le système d’assistance extra-corporelle type Thoratec (gauche-gauche ou biventriculaire), assez souvent utilisé. Des pompes plus simples et plus facilement implantables sont en cours d’étude clinique.
Figure 2. Place de l’assistance circulatoire.
Assistance mécanique externe type Thoratec
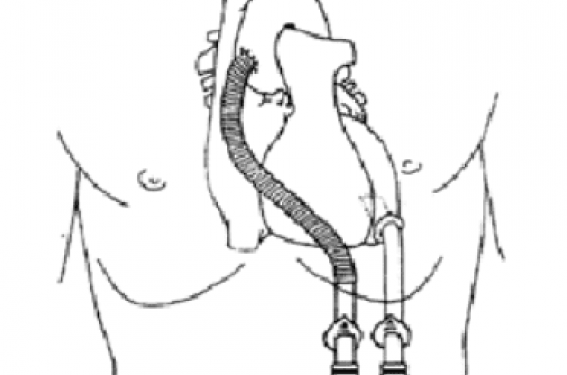
Thoratec est un système pneumatique qui fournit une prise en charge uni- ou biventriculaire grâce à des prothèses de type sacs placées en position paracorporelle et reliées à une console ou à un système portable. Il se compose de 3 éléments séparés : les canules, une pompe et une console. Selon le site d’insertion au niveau du patient, on peut définir une canulation atriale droite-gauche (dans l’oreillette), une canulation artérielle (dans la racine de l’aorte ou dans le tronc de l’AP) et une canulation apicale (dans la pointe du VG) (figure 3).
Figure 3. Système Thoratec : prise en charge univentriculaire (à gauche) ou biventriculaire (à droite).
La pompe assure un débit pulsatile grâce à un système pneumatique. Chaque ventricule est de type sac, constitué d’une chambre souple en polyuréthane insérée dans une coque rigide de polysulfane. Le sac est activé par un déplacement d’air dans l’enceinte rigide. Deux orifices valvés donnent à l’écoulement un sens unidirectionnel.
L’avantage essentiel des dérivations pneumatiques tient au traumatisme sanguin minime des pompes à sac. Un second avantage tient à la rapidité et à la simplicité de la mise en œuvre après sternotomie. Des canules peuvent être positionnées simplement sans qu’il soit absolument nécessaire de recourir à une circulation extracorporelle. Il sera plus facile de choisir ce type d’assistance dans un contexte d’urgence avec dysfonction ventriculaire globale plutôt qu’un système intracorporel type Novacor.
L’inconvénient des dérivations extracorporelles pneumatiques réside :
• dans la localisation extracorporelle des ventricules, avec notamment le risque de contamination infectieuse des orifices cutanés,
• dans l’encombrement de la console (volumineux générateur délivrant l’air comprimé). Cependant, ce système est désormais disponible sous forme portable, d’un faible encombrement (7 kg), il assure une assistance uni- ou biventriculaire et se substitue à la console.
Indications d’assistance mécanique circulatoire
Assistance mécanique en général temporaire pont vers la transplantation. L’indication d’assistance mécanique circulatoire est posée chez un patient jugé bon candidat à la transplantation cardiaque, qui échappe à un traitement médical maximal faisant usage d’une combinaison de médicaments inotropes et de l’optimisation des pressions de remplissage. Cette situation se traduit par des critères cliniques précis : PAS < 90 mm Hg, PA moyenne < 70 mmHg, tachycardie permanente, diurèse horaire < 30 cm3/h. Ces critères sont confirmés par l’hémodynamique : index cardiaque < 2 ml/min/m2, différence artérioveineuse élargie à 8, PA pulmonaire moyenne > 30 mmHg, pression capillaire moyenne à 18 mmHg.
Les circonstances étiologiques de ces situations hémodynamiques réfractaires sont diverses : phase aiguë d’infarctus sans possibilité de revascularisation chirurgicale, myocardite aiguë, évolution aiguë d’une cardiomyopathie chronique ou valvulaire. Dans tous les cas, la décision d’implantation doit concerner un patient jugé bon candidat à la transplantation selon les critères connus (âge, absence d’hypertension artérielle pulmonaire non réversible, absence de contre indication à l’immunosuppression).
Ainsi, la sélection des patients à une assistance mécanique circulatoire est un élément clé de succès. L’indication, sans être trop précoce, ne doit pas non plus être tardive. Il est essentiel d’envisager la mise en place d’une assistance avant que ne survienne la situation de défaillance multiorganes irréversible. Pour cela, il est important de connaître les facteurs prédictifs de décès sous assistance qui, selon McCarthy, sont la ventilation mécanique préalable, la diurèse horaire < 30 cm3/h, et le taux de créatinine et d’urée sanguine. Une fois le patient bien sélectionné, cette stratégie thérapeutique a prouvé son efficacité. Dans l’expérience de Frazier portant sur 75 patients en insuffisance cardiaque réfractaire placés sous assistance, comparés à 33 patients témoins traités médicalement, la mortalité sous assistance en attente d’un greffon a été de 28 contre 63 % dans le groupe témoin, soit une réduction de mortalité de 55 % dans le groupe assisté. Par ailleurs, la survie après transplantation cardiaque est significativement supérieure à 1 an par rapport au groupe témoin (91 vs 67 %, p < 0,001).
La récupération de la dysfonction viscérale sous assistance est observée dans un délai de 2 à 5 semaines. Ce délai de récupération des différentes fonctions est, pour certains, l’élément de succès du pont à la transplantation plus que la durée d’attente elle-même.
Choix du système en pratique. Choisir le type d’assistance adaptée au patient impose de faire une analyse précise du contexte étiologique, de la possibilité de récupération myocardique et de la fonction ventriculaire droite.
L’expérience d’un système intracorporel type Novacor a prouvé une grande efficacité clinique et hémodynamique. Il s’agit probablement d’un système à proposer dans une situation de cardiomyopathie dilatée chronique sans atteinte ventriculaire droite chez un patient de moins de 50 ans, dont les caractéristiques de poids, de taille et de groupe sanguin conduisent à privilégier le système le plus efficace en termes de possibilité de réhabilitation en vue d’une attente prolongée. D’autres systèmes plus simples sont en cours d’étude.
En revanche, dans tous les cas de défaillance globale ou avec atteinte ventriculaire droite, un système paracorporel type Thoratec est indiqué car moins lourd sur l’acte chirurgical et n’excluant pas la possibilité de sevrage une fois la période critique initiale passée. Il est maintenant clairement établi que les patients avec dysfonction ventriculaire droite chronique ne bénéficient pas d’une assistance ventriculaire gauche isolée et 19 % des patients inclus dans l’essai multicentrique Novacor ont nécessité l’implantation d’une assistance ventriculaire droite. Cependant, la survenue d’une dysfonction ventriculaire droite sous assistance gauche reste difficilement prévisible, même par l’étude de l’évolution hémodynamique.
Principales complications potentielles des assistances mécaniques circulatoires
Infections
Leur incidence varie, selon les séries, de 18 à 27 % et est clairement en relation avec la durée de l’assistance mécanique. Il s’agit le plus souvent d’une contamination le long des canules, au niveau des orifices cutanés pour les systèmes type Thoratec, ou d’une infection de la poche elle-même pour les systèmes Novacor. Dans ce dernier cas, la mise en place d’un lavage-drainage est systématique ainsi que l’instauration d’une antibiothérapie sélective adaptée. Cette complication grave ne contre-indique cependant pas la transplantation si elle n’a pas de retentissement systémique et elle ne semble pas modifier la survie après transplantation cardiaque. Pour les systèmes Thoratec, l’utilisation de canules transcutanées spécialement revêtues constitue un certain progrès prolongeant l’attente de la transplantation.
Accidents thromboemboliques
La formation de thrombus, et par voie de conséquence d’embolie systémique chez les patients sous assistance ventriculaire, est la conséquence d’une stase sanguine, de l’existence de surface artificielle et d’une anticoagulation inadéquate.
En pratique
L’insuffisance cardiaque aiguë, cause importante de décès des insuffisants cardiaques, concernera de plus en plus une population âgée pour laquelle aujourd’hui peu d’options autres que médicamenteuses sont à proposer. Le développement de nouvelles méthodes d’assistance a amélioré la prise en charge chez des patients réfractaires aux inotropes.
Attention, pour des raisons réglementaires ce site est réservé aux professionnels de santé.
pour voir la suite, inscrivez-vous gratuitement.
Si vous êtes déjà inscrit,
connectez vous :
Si vous n'êtes pas encore inscrit au site,
inscrivez-vous gratuitement :