Mise au point
Publié le 30 nov 2014Lecture 5 min
Peut-on éviter la reconnexion des veines pulmonaires ?
S. ABBEY, D. GRAS, J.-P. CEBRON, Nouvelles Cliniques Nantaises, Nantes
L’ablation de la fibrillation atriale (FA) paroxystique a connu un véritable essor depuis l’identification du rôle primordial des veines pulmonaires (VP) comme facteur déclenchant. La déconnexion électrophysiologique des VP est la cible actuellement reconnue, l’encerclement antral semblant plus efficace que la déconnexion segmentaire(1).
L’efficacité à 1 an est estimée à environ 80 % avec 40 % de procédures « redux ».
Lors des récidives, il est souvent constaté une reconnexion atrioveineuse.
Le préambule pour assurer une déconnexion pérenne est de documenter rigoureusement les blocs d’entrée et de sortie, en positionnant le cathéter circulaire à l’ostium des VP.
Le délai d’observation après isolation est un élément important à considérer, même s’il est difficile à respecter au quotidien. Les reconnexions sont surtout constatées durant les 30 minutes après l’isolation initiale(2). Un délai de surveillance de 20 minutes est inscrit dans les recommandations américaines(3).
Pour réduire la reconnexion veineuse, deux procédures ont émergé pour identifier les régions où l’ablation est incomplète (gaps).
La première technique est un test pharmacologique qui permet de différencier un bloc permanent d’une conduction dormante entre l’oreillette et la veine (le tissu est viable, mais la conduction latente).
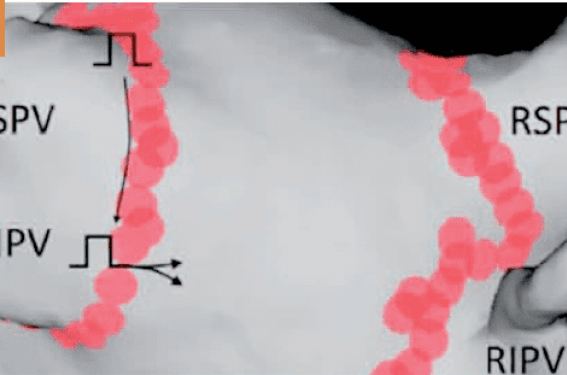
L’identification de cette conduction dormante est définie par la présence d’une conduction veinoatriale, transitoire ou permanente, révélée après injection d’adénosine (Striadyne 10 à 20 mg, pour obtenir au moins une onde P bloquée : figure 1). La disparition de ces conductions induites après complément d’ablation permet une amélioration pronostique significative(4).
Figure 1. Reconnexion transitoire (étoiles) après injection d’adénosine.
L’étude randomisée ADVICE(5) a montré qu’avec ce test, des veines dormantes sont démasquées chez 53 % des patients (et 21 % des VP) après ablation. L’ablation complémentaire pour déconnecter ces veines dormantes permet une efficacité à 1 an (absence de flutter/FA après une seule procédure) de 69,4 % des patients contre 42,3 % pour les patients sans ablation complémentaire et 55,7 % des patients sans conduction dormante (réduction du risque relatif (RRR) : 56 %).
Concernant le test pharmacologique utilisé, l’adénosine semble supérieure à l’isoprotérénol(6). Ce test est applicable également après cryoablation, même si les signaux sont plus difficiles à analyser avec le cathéter guide Achieve™ (Medtronic)
La stratégie alternative « pace/ablate » consiste à s’assurer que le tissu est non excitable sur la ligne d’ablation et vérifier l’absence de capture lors de la stimulation sur chaque site de tir.
En effet, la déconnexion des VP par encerclement large antral reste un défi compte tenu d’une anatomie parfois complexe et de la difficulté de faire des applications avec une position stable du cathéter. Il est difficile de s’assurer que les lésions sont complètement transmurales et continues. De plus, en cas de persistance de conduction atrioveineuse après encerclement, il est souvent compliqué d’identifier précisément le gap à l’origine de la connexion si l’on veut éviter de faire des applications trop ostiales (les fibres sont parfois entrelacées entre veine supérieure et inférieure, avec des trajets complexes).
Après avoir effectué un encerclement anatomique, une stimulation par le pôle distal du cathéter d’ablation est effectuée le long de la ligne d’encerclement des veines (stimulation à 10 mA x 2 ms) en s’aidant des caractéristiques du signal sur le site de stimulation et de la cartographie 3D (figure 2). Si le myocarde est toujours excitable au site de stimulation, un tir complémentaire est effectué sur le point (voire sur les sites adjacents) jusqu’à obtenir une perte de capture. Cette technique permet une amélioration significative du taux de succès des procédures si on la compare à la seule obtention d’un bloc bidirectionnel (absence de FA/flutter : 82 % vs 52 % à 1 an(7)).
Figure 2. Exemple de capture (A), absence de capture après tir complémentaire (B) (d’après Andrade(8)).
L’utilisation de cette technique permet une diminution significative de l’incidence des conductions dormantes révélées par un test à l’adénosine(8).
Ces deux tests semblent équivalents en termes d’efficacité à long terme(8).
La création de lésions d’ablation permanentes devrait permettre d’obtenir une déconnexion veineuse pérenne. En plus de la durée de tir et de la puissance délivrée, qui sont les paramètres usuels programmés, la mesure du contact entre le tissu et l’électrode s’impose comme un élément déterminant d’efficacité. La mesure nécessite l’utilisation de cathéters dédiés (SmartTouch® de Biosense, TactiCath™de St. Jude Medical). Ces stratégies ont été validées par les études TOCCATA(9), EFFICAS(10) et SMART-AF(11). Le contact peut être apprécié par la mesure de la force moyenne (en grammes) ou par l’intégrale force/temps FTI (aire sous la courbe force/temps). Il est primordial d’obtenir un contact suffisant entre l’électrode et le tissu dès la première application sur chaque site afin d’éviter l’œdème induit par l’ablation qui peut limiter l’efficacité des tirs complémentaires.
Les principaux critères qui semblent prédictifs de tirs efficaces sont, en dehors de la puissance délivrée :
- force > 18-20 g (efficacité si > 10 g, tout en restant < 80-100 g pour éviter les perforations) ;
- FTI > 400-500 ;
- stabilité du cathéter (le contact doit être supérieur au contact ciblé pendant plus de 80 % de la durée du tir).
L’utilisation de ces cathéters permet d’augmenter significativement l’efficacité à 1 an (88 % vs 66 % en l’absence de mesure de contact), en diminuant l’incidence des veines dormantes(12).
D’autres marqueurs de lésions sont également à l’étude (modifications du signal unipolaire, variation de l’impédance, etc.).
Ces paramètres peuvent être intégrés dans le module VisiTag™(système Carto® 3, Biosense), qui permet une notification automatique des points d’ablation (tags) effectués selon le contact, la durée du contact ciblé, le FTI, etc. Ce logiciel devrait permettre d’harmoniser les pratiques.
Dans notre centre, les paramètres utilisés nécessaires à la visualisation d’un tag sont : force > 10 g, FTI > 400 en région postérieure (maximum 25 W), 800 en région antérieure (maximum 30 W).
Concernant la cryoablation, les résultats avec le ballon de nouvelle génération semblent comparables à l’utilisation de la radiofréquence avec contact(13).
Conclusion
Pour éviter la reconnexion veineuse et diminuer les récidives, il semble primordial d’effectuer, en fin d’intervention, un test pharmacologique et/ou stimuler sur la ligne d’ablation.
L’utilisation des cathéters contacts devrait progresser avec leur amélioration attendue en termes de maniabilité.
Ces apprentissages et l’intégration de nouveaux outils font espérer des progrès rapides en termes d’efficacité des procédures.
Attention, pour des raisons réglementaires ce site est réservé aux professionnels de santé.
pour voir la suite, inscrivez-vous gratuitement.
Si vous êtes déjà inscrit,
connectez vous :
Si vous n'êtes pas encore inscrit au site,
inscrivez-vous gratuitement :


